甲、乙、丙、丁4种物质分别含2种或3种元素,它们的分子中各含18个电子,甲是气态氢化物,在水中分步电离出两种阴离子,下列推断合理的是
| A.某钠盐溶液含甲电离出的阴离子,则该溶液显碱性,只能与酸反应 |
| B.乙与氧气的摩尔质量相同,则乙一定含有极性键和非极性键 |
| C.丁和甲中氢元素质量比相同,则丁中一定含有氧元素 |
| D.丙中含有第2周期ⅣA族的元素,则丙一定是甲烷的同系物 |
如图所示,集气瓶内充满某气体,置于明亮处,将滴管内的水挤入集气瓶后,烧杯中的水会进入集气瓶,集气瓶内气体可能是
①NH3 B.②N2、H2③NO2、O2 ④SO2 ⑤CH4、Cl2
A. ①②③④ B. ②③④⑤ C. ①③④⑤ D. ①②③⑤
已知反应 是可逆反应。设计如图装置(
是可逆反应。设计如图装置( 、
、 均为石墨电极),分别进行下述操作。
均为石墨电极),分别进行下述操作。
Ⅰ.向B烧杯中逐滴加入浓盐酸
Ⅱ.向B烧杯中逐滴加入40% NaOH溶液
结果发现电流计指针均发生偏转.据此,下列判断正确的是
| A.操作Ⅰ过程中,C1为正极 |
| B.操作Ⅱ过程中,盐桥中的K+移向B烧杯溶液 |
| C.Ⅰ操作过程中,C2棒上发生的反应为:AsO43-+2H++2e-=AsO33-+H2O |
| D.Ⅱ操作过程中,C1棒上发生的反应为:2I――2e-=I2 |
下图所示是验证氯气性质的微型实验,a、b、d、e是浸有相关溶液的滤纸。向KMnO4晶体滴加一滴浓盐酸后,立即用另一培养皿扣在上面。
已知:2KMnO4+16HCl→2KCl+5Cl2↑+2MnCl2+8H2O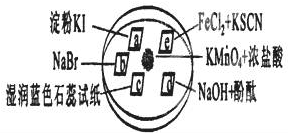
对实验现象的“解释或结论”正确的是
| 选项 |
实验现象 |
解释或结论 |
| A |
a处变蓝,b处变红棕色 |
氧化性:Cl2>Br2>I2 |
| B |
c处先变红,后褪色 |
氯气与水生成了酸性物质 |
| C |
d处立即褪色 |
氯气与水生成了漂白性物质 |
| D |
e处变红色 |
还原性:Fe2+>Cl- |
当光速通过下列分散系时,能产生丁达尔效应的是
| A.NaCl溶液 | B.泥水 | C.盐酸 | D.氢氧化铁胶体 |
下列各组离子中,在碱性溶液中能大量共存,且溶液为无色透明的是
| A.K+ MnO4- Cl- SO42- | B.Na+ AlO2- Cl-SO42- |
| C.SO42-Na+HCO3-Ba2+ | D.Na+ NO3- NH4+ SO42- |