A-H及X均为中学化学常见物质, X是一种金属单质,A、B是非金属单质且A在常温下为气体。它们在一定条件下有如下转化关系(图中条件均已略去)。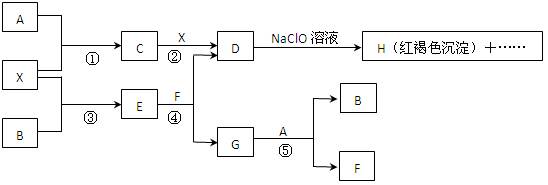
试回答下列问题:
(1)写出C物质的化学式 ;
(2)在上述①-⑤ 反应中肯定不属于氧化还原反应的是 (填编号);
反应中肯定不属于氧化还原反应的是 (填编号);
(3)指出元素X在元素周期表中的位置: ;
(4)请写出反应④和⑤的离子方程式:④ ,
⑤ ;
(5)用离子方程式表示在D溶液中加入NaClO溶液产生红褐色沉淀的原因:
。
1 mol气态钠离子和1 mol气态氯离子结合生成1 mol氯化钠晶体释放出的热能为氯化钠晶体的晶格能。
(1)下列热化学方程中,能直接表示出氯化钠晶体格能的是。
| A.Na+(g) + Cl-(g) → NaCl(s);△Q | B.Na(s) + Cl2(g) → NaCl(s);△Q1 |
| C.Na(s) → Na(g); △Q2 | D.Na(g)-e-→ Na+(g); △Q3 |
E.Cl2(g) → Cl(g);△Q4 F.Cl(g) + e-→ Cl-(g);△Q5
(2)写出△Q1与△Q、△Q2、△Q3、△Q4、△Q5之间的关系式。
观察图a和图b,根据盖斯定律,写出△H1、△H2、△H3、△H4、△H5和△H6的关系。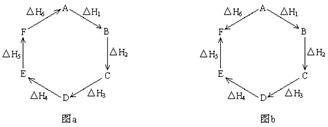
图a:;图b:。
由金红石(TiO2)制取单质Ti,涉及到的步骤为: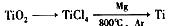
已知:① C(s) + O2(g) ="=" CO2(g); △H = -393.5 kJ•mol-1
② 2CO(g) + O2(g) ="=" 2CO2(g); △H = -566 kJ•mol-1
③ TiO2(s) + 2Cl2(g) ="=" TiCl4(s) + O2(g); △H =" +141" kJ•mol-1
(1)则TiO2(s) + 2Cl2(g) + 2C(s)="=" TiCl4(s) + 2CO(g) 的△H = _________________。
(2)反应TiCl4 + 2Mg ="=" 2MgCl2 + Ti 在Ar气氛中进行的理由是_____________。
液化气的主要成分是丁烷,当10g丁烷完全燃烧生成CO2和液态水时,放出热量为500kJ,写出丁烷燃烧的热化学方程式:丁烷的燃烧热为kJ /mol。已知1mol液态水汽化时需要吸收44kJ的热量,则C4H10(g)+13/2O2(g)="==" 4CO2(g)+5H2O(g);△H="=" kJ /mol。
10 g硫磺在 O2中完全燃烧生成气态SO2,放出的热量能使 500 g H2O温度由18℃升至62.4℃,则硫磺的燃烧热为,热化学方程式为。