.下表是某食用碘盐包装袋上的部分说明:
| 配 料 |
食盐、碘酸钾、抗结剂 |
| 碘含量 |
35±15mg/kg |
| 储藏方法 |
密封、避光、防潮 |
| 食用方法 |
烹饪时,待食品熟后加入碘盐 |
请回答下列问题:
(1)下列说法正确的是 。
A.碘酸钾易挥发 B.高温会导致碘的损失
C.用淀粉就能直接检验碘盐中的碘酸钾 D.碘酸钾可氧化氯化钠
(2)碘酸钾与碘化钾在酸性条件下发生如下反应:KIO3+KI+H2SO4→K2SO4+I2+H2O(未配平),该化学方程式配平后系数依次为 。
w.该反应的还原剂为 ;1mol KIO3完全反应转移的电子总数为 。
(3)碘不能多也不能少。已知:I2+2S2O32-=2I-+S4O62-,我校化学兴趣小组测定某食用碘盐中碘的含量。其步骤为:
①准确称取w g食盐,加适量蒸馏水使其完全溶解;②用稀硫酸酸化所得溶液,加入足量KI溶液,使KIO3与KI反应完全;③以淀粉为指示剂,逐滴加入物质的量浓度为1.0×11-3mol·L-1的Na2S2O3溶液20.0mL,恰好反应完全。则所测盐中碘的含量是(以含w的代数式表示) mg/kg。
A、B、C、D四种芳香族化合物都是某些植物挥发油中的主要成分,有的是药物,有的是香料。它们的结构简式如下所示: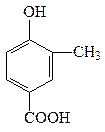
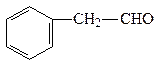
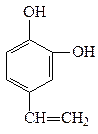

A BC D
(1)A中的含氧官能团名称是。
(2)B与足量氢气充分反应的产物的结构简式为。
(3)D发生聚合反应的产物的结构简式为。
(4)A能与乙醇发生反应生成一种有特殊香味的物质,请写出该反应的方程式:
。
(5)关于上述四种物质的说法中正确的是。
A.都能与Na反应放出H2
B.C、D均能使溴的四氯化碳溶液褪色
C.A和C均能与NaHCO3溶液反应放出CO2
D.1molC最多能与4molBr2发生反应
元素周期表反映了元素性质的周期性变化规律。请根据短周期元素在周期表中的位置、结构和相关性质,回答下列问题:
(1)第VIA族元素形成的氢化物中沸点最高的是____________(用分子式表示),原因是____________________,该分子的空间构型为______________。
(2)第二周期元素中,除Be、B、Ne三种元素外,其他元素的氢化物沸点如表1所示,其中E的化学式为 ;第三周期元素单质的熔点(℃)变化如图a所示,其中h的元素符号为 。(表1)
| 氢化物 |
A |
B |
HF |
D |
E |
| 沸点/℃ |
1317 |
100 |
19.5 |
 33.35 33.35 |
 164 164 |
(3)第二、第三周期的某些元素能形成单质甲和化合物乙,它们具有图b所示的结构单元,甲和乙的晶体类型相同,甲的某种同素异形体与乙在高温时能发生置换反应生成h的单质和CO。若该反应生成的h的单质含有1 mol共价键,则参加反应的乙的质量为_______________g。
(4)碳元素的某种单质具有平面层状结构,该单质的名称为__________;同一层中的原子构成许多的正六边形,单质与熔融的钾相互作用,形成某种青铜色的物质(其中的元素钾用“●”表示),原子分布如图c所示,该物质的化学式为 。
在①渗析②盐析③聚沉④溶胶⑤凝胶⑥布朗运动⑦电泳⑧丁达尔效应⑨中和⑩水解中选择适当的词语填入下列每小题的空格中(填编号)。
(1)用平行可见光照射肥皂水,从侧面可以见到光带。这种现象称为 。
(2)冷却热的肥皂水并使之全部固化后的物质叫 。
(3)在肥皂水中加入酚酞变成红色,说明高级脂肪酸根离子发生了 。
(4)在Fe(OH)3胶体中加入(NH4)2SO4,产生红褐色沉淀,这种现象叫做 。
(5)用半透膜把制取的Fe(OH)3胶体中含有的NaCl分离出去的方法叫做 。
现有Cu2+、Cl―、Na+、SO42―、Zn2+两两组成的电解质溶液若干种,可选用铜电极、铂电极、锌电极进行电解实验。
(1)以铜为阳极电解_________或____________溶液,均可得到氢氧化物沉淀。
(2)要使电解过程中溶质的组成和质量不变,而溶液浓度增大,又无浑浊,应以
__________为阳极电解_____________溶液,化学方程式为_______________________。
(3)要使电解过程中溶液浓度改变,而溶剂质量不变,应以铂电极为阳极电解___________溶液,或以_________为阳极电解________溶液,前者反应的化学方程式是_________________________。
(4)使反应Cu+2H2O==Cu(OH)2 ↓+H2 ↑ 得以进行而不发生其它反应,可选用______________为阳极电解__________或____________溶液
(5)以铜为阳极电解ZnSO4溶液,阴极上一般有___________逸出,在________极区首先会有__________色沉淀,电解时间较长时,会有______色沉淀出现。
(1)请将5种物质:N2O、FeSO4、Fe(NO3)3、HNO3和Fe2(SO4)3分别填入下面对应的横线上,组成一个未配平的化学方程式。
_________+__________→__________+__________+__________+H2O
(2)反应物中发生氧化反应的物质__________,被还原的元素是_________。
(3)反应中1 mol氧化剂_______(填“得到”或“失去”)___________ mol电子。
(4)请将反应物的化学式及配平后的系数填入下列相应的位置中,并用单线桥表示: