在一次学生实验中,学生用带有氧化膜的铝片和稀硫酸反应,发现铝片和稀盐酸、稀硫酸反应发现铝片和稀盐酸反应现象明显,而和稀硫酸几乎不反应。这和“铝能跟稀盐酸或稀硫酸反应生成氢气”不一致,是什么原因呢?是试剂、药品出了问题吗?为了寻找原因,某学生在教师的指导重新用浓盐酸配制了一定浓度的溶液,然后加入一块纯度≥99.5%的铝片验证是否确实存在上述现象,实验结果如下表
无论是用5%H2SO4还是用10%H2SO4,均无明显现象。其结论还是与“铝能跟稀硫酸或稀盐酸反应生成氢气”不相符合。
问题1:为了探索“铝与稀盐酸和稀硫酸反应的差异原因”,你能对问题的答案作出哪些假设或猜想:
假设一:Cl-能
假设二:SO42-能
问题二:为了论证上述假设,你设计的实验方案是:(探究过程)_______________
乙炔(化学式为
)是一种重要的有机化工原料,以乙炔为原料在不同的反应条件下可以转化成多种化合物。乙炔气体和氧气反应能产生高温火焰(氧炔焰),工人师傅常用氧炔焰切割或焊接金属构件。现在让我们一起对乙炔燃烧(氧炔焰)的产物进行探究。
【查阅资料】当还原性气体中混有水蒸汽时,则难以还原氧化铜。
【提出问题】乙炔燃烧的产物中除水外主要还有哪些物质?
【假设与猜想】猜想:①一定有;②可能有一氧化碳。
【实验设计】根据上述两种物质的猜想设计如下实验:
(1)在氧炔焰上方罩一个内壁附着有的大烧杯,观察现象。
(2)将乙炔燃烧的产物依次通入足量的澄清石灰水和足量的浓硫酸,将剩余气体通过炽热的氧化铜,若氧化铜变红,说明有(填写化学式)。
【证据与结论】
实验(1):观察到烧杯内壁附着的,则猜想①成立。反应的化学方程式为:。
实验(2):若氧化铜变红,则猜想②成立。
【分析与交流】实验(2)时,若将乙炔燃烧的产物依次通入足量的浓硫酸和足量的澄清石灰水,再将剩余气体通过炽热的氧化铜,此时氧化铜不变红,能否证明猜想②不成立?(填"能"或"不能")。
可用作催化剂和外伤止血剂.某实验兴趣小组利用
腐蚀电路铜板后的溶液(主要成分为
、
)进行了氯化铁回收实验.
实验一:(如图1)
(1)写出步骤①中发生的化学方程式,此反应的基本类型是.
(2)步骤②中的操作a名称是;步骤③中加入稀盐酸的目的是.
实验二:该实验小组同学通过查阅资料,又进行了另一种尝试.
【阅读资料】不同金属氢氧化物可以在不同的pH范围内从溶液中沉淀析出,工业上利用调节溶液pH的方法,使金属氢氧化物依次沉淀,结合过滤等操作,进行物质分离.
如表是氢氧化铁与氢氧化铜开始沉淀与沉淀完全的
.
|
|
|
|
| 开始沉淀的pH |
1.9 |
4.7 |
| 沉淀完全的pH |
3.2 |
6.7 |
(3)如图2,步骤b加入
消耗溶液甲中的
,使溶液pH增大到所需范围,请写出盐酸与氧化铜反应的化学方程式;你认为步骤b调节溶液的pH到 (数值范围)比较合适.
(4)该实验需要用pH试纸测量溶液的pH,请将pH试纸的使用方法补充完整:,,把试纸显示的颜色与标准比色卡比较,读出该溶液的
.
(5)
溶液容易生成
发生变质,在保存
溶液时,常向
溶液中加入某种酸,以防止
溶液变质,你认为选用(用字母表示)最合理.
| A. |
稀硝酸 |
B. |
稀硫酸 |
C. |
稀盐酸 |
D. |
稀醋酸. |
请根据材料与要求回答下列问题: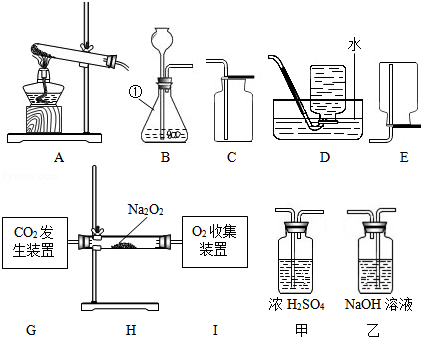
(1)如图1中标号为①的仪器名称是,实验室用高锰酸钾制取并收集氧气,可选用图中的(填字母)装置.
(2)实验室用高锰酸钾制取氧气时,会用到一团棉花,这团棉花的作用是,生产氧气的化学方程式是.
【阅读资料】过氧化钠(化学式为
)是一种浅黄色固体粉末,二氧化碳与过氧化钠反应可生成氧气,反应的化学方程式为
,潜艇利用该反应原理供氧.
(3)刘丰同学想验证潜艇供氧原理,请写出实验室用石灰石制取
的化学方程式.
(4)用如图2装置制取的氧气中,含有少量二氧化碳气体,应该在H与I之间添加("甲"或"乙")装置进行气体净化;该实验中,装置H的玻璃管里固体颜色会由浅黄变成.
张宁和刘明同学学习完酸、碱、盐后发现:碱溶液能使酚酞溶液变红,
溶液也能使酚酞溶液变红。通过学习知道,碱溶液使酚酞溶液变红,是因为碱在水中离解出
,那么
溶液中究竟是哪种粒子使酚酞溶液变红呢?请你帮助他俩完成实验探究。
【提出问题】
属于(填"酸"、"碱"、"盐"),为什么能使酚酞溶液变红?
【进行猜想】
(1)
使酚酞溶液变红。
(2)水分子使酚酞溶液变红。
(3)使酚酞溶液变红。
【设计实验】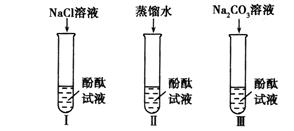
(1)实验Ⅰ的目的是为了验证猜想不成立。
(2)刘明同学认为实验Ⅱ没必要做,他的理由是。
(3)实验Ⅲ滴入
溶液,振荡,酚酞试液变红。向变红后的溶液中滴加
溶液至过量,振荡,出现的现象是,反应的化学方程式是。(提示:
溶液呈中性)
(4)由实验Ⅰ、Ⅱ、Ⅲ得出猜想(3)正确。张宁对此结论有些质疑,于是他查阅资料。
【查阅资料】
溶液中,
和
发生如下反应:
【得出结论】 溶液中使酚酞溶液变红的粒子是。
化学是以实验为基础的自然科学,下图所示为实验室常用的实验装置:
据此回答:
(1)实验室若用A装置制取氧气,写出反应的化学方程式。
(2)实验室通常用石灰石和稀盐酸反应制取
,所需要的装置组合是(填装置序号);也可以用碳酸氢钠(
)固体加热分解(产物为碳酸钠、二氧化碳和水)来制取,该反应的化学方程式为。
(3)F装置可用来测量生成的
气体的体积,其中在水面上放一层植物油的目的
是。
(4)实验室若检验
应选择装置,其反应的化学方程式为。