以NA代表阿伏加德罗常数,则关于热化学方程式 C2H2 ( g ) +5/2O2 ( g ) = 2CO2 ( g )+H2O ( l ) △H =" —1300kJ" / mol 的说法中,正确的是
| A.当10 NA个电子转移时,该反应放出1300kJ的能量 |
| B.当1 NA个水分子生成且为液体时,吸收1300kJ的能量 |
| C.当2 NA个碳氧共用电子对生成时,放出1300kJ的能量 |
| D.当8 NA个碳氧共用电子对生成时,放出1300kJ的能量 |
下列有关电负性的说法中正确的是( )
| A.主族元素的电负性越大,元素原子的第一电离能一定越大 |
| B.在元素周期表中,元素电负性从左到右越来越大 |
| C.金属元素电负性一定小于非金属元素电负性 |
| D.在形成化合物时,电负性越小的元素越容易显示正价 |
图中是部分短周期元素化合价与原子序数的关系图,下列说法正确的是( )
| A.原子半径:Z>Y>X |
| B.气态氢化物的稳定性:R﹤W |
| C.WX3和水反应形成的化合物是离子化合物 |
| D.Y和Z两者最高价氧化物对应的水化物能相互反应 |
下列叙述错误的是()
(1)若R的含氧酸的酸性大于Q的含氧酸的酸性,则非金属性R大于Q
(2)阴、阳离子通过静电吸引形成的化学键叫离子键
(3)H2O、H2S、H2Se的相对分子质量增大,所以熔沸点依次升高
(4)液态氟化氢中存在氢键,所以其分子比氯化氢更稳定
(5)都是由非金属元素形成的化合物只能是共价化合物
| A.全部 | B.(1)(2)(3)(4) |
| C.(1)(2)(3)(5) | D.(2)(3)(4) |
下列化学用语表示正确的是( )
A.甲基的电子式: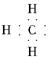 |
B.氮原子的轨道表示式: |
| C.氯离子的最外层电子排布:3s23p6 |
D.硫离子的结构示意图: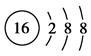 |
下列叙述中,错误的是()
| A.苯与浓硝酸、浓硫酸共热并保持55-60℃反应生成硝基苯 |
| B.苯乙烯在合适条件下催化加氢可生成乙基环己烷 |
| C.乙烯与溴的四氯化碳溶液反应生成1,2-二溴乙烷 |
| D.甲苯与氯气在光照下反应主要生成2,4-二氯甲苯 |