下列措施不能有效防止钢铁腐蚀的是
| A.在钢铁中加入铬制成不锈钢 | B.把钢铁零件放在机油中保存 |
| C.在较小钢铁制品的表面包裹塑料 | D.在大型铁壳船表面喷涂油漆并钉上铜块 |
在一密闭容器中,反应 aA(g) bB(g)达平衡后,保持温度不变,将容器体积缩小一倍,当达到新的平衡时,A的浓度变为原来的1.8倍,则()
bB(g)达平衡后,保持温度不变,将容器体积缩小一倍,当达到新的平衡时,A的浓度变为原来的1.8倍,则()
| A.平衡向正反应方向移动了 | B.平衡向逆反应方向移动了 |
| C.物质A的质量分数增加了 | D.a<b |
实验室现有3种指示剂,其pH变色范围如下:甲基橙:3.1~4.4石蕊:5.0~8.0酚酞:8.2~10.0用0.1000 mol/L NaOH溶液滴定未知浓度的CH3COOH溶液,反应恰好完全时,下列叙述中正确定是( )
| A.溶液呈中性,可选用石蕊或酚酞作指示剂 |
| B.溶液呈中性,必选用石蕊作指示剂 |
| C.溶液呈碱性,可选用甲基橙或酚酞作指示剂 |
| D.溶液呈碱性,可选用酚酞作指示剂 |
0.1mol/L的K2CO3溶液中,由于CO32-的水解,使得c(CO32-)<0.1mol/L。如果要使c(CO32-)更接近于0.1mol/L,可以采取的措施是 ( )
| A.加入少量盐酸 | B.加入适量的水 | C.加入适量的NaOH | D.加热 |
在由水电离出的c(H+)=10-13 mol·L-1的溶液中,一定能大量共存的离子组( )
| A.K+、Na+、HCO3-、Cl- | B.K+、Fe3+、Br-、I- |
| C.Na+、Cl-、NO3-、SO42- | D.NH4+、Al3+、Cl-、SO42- |
下列说法不正确的是()
| A.用稀盐酸洗涤AgCl沉淀比用水洗涤损耗AgCl小; |
| B.沉淀反应中常加过量的沉淀剂,其目的是使沉淀完全; |
C.对于Al(OH)3(s)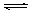 Al(OH)3(aq) Al(OH)3(aq) 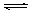 Al3++3OH-,前者为溶解平衡,后者为电离平衡; Al3++3OH-,前者为溶解平衡,后者为电离平衡; |
| D.除去溶液中的Mg2+,用OH-沉淀Mg2+比用CO32-效果好,说明Mg(OH)2的溶解度比MgCO3大 |