设NA为阿伏加德罗常数的数值,下列说法正确的是()
| A.常温下,23g NO2含有NA个氧原子 |
| B.1 L 0.1 mol·L-1的氨水含有0.1NA个OH- |
| C.标准状况下,22.4 L CCl4含有NA 个CCl4分子 |
| D.1 mol Fe2+与足量的H2O2溶液反应,转移2NA个电子 |
已知某合金(仅含铜、铁)中铜和铁的物质的量之和为y mol,其中Cu的物质的量分数为a,将其全部投入50 mL b mol·L-1的硝酸溶液中,加热使其充分反应(假设NO是唯一的还原产物)。下列说法正确的是()
| A.若金属没有剩余,反应中转移的电子数目为2y NA |
| B.若金属全部溶解,则溶液中一定含有Fe3+ |
| C.当溶液中金属离子只有Fe3+、Cu2+时,则a与b的关系为:b≥80 y(1-a/3) |
| D.若金属全部溶解,且产生336 mL气体(标准状况),则b=0.3 |
已知实验:①0.1 mol·L-1 AgNO3溶液和0.1 mol·L-1 NaCI溶液等体积混合得到浊液a,过滤得到滤液b和白色沉淀;② 向滤液b中滴加0.1 mol·L-1 KI溶液,出现浑浊;③ 向沉淀c中滴加0.1 mol·L-1 KI溶液,沉淀变为黄色。下列分析不正确的是()
A.浊液a中存在沉淀溶解平衡:AgCl(s) Ag+(aq)+Cl—(aq) Ag+(aq)+Cl—(aq) |
| B.滤液b中不含有Ag+ |
| C.③中颜色变化说明AgCl 转化为AgI |
| D.实验可以证明AgI比AgCl更难溶 |
向某密闭容器中加入0.6 mol A、0.2 mol C和一定量的B三种气体。一定条件下发生反应,各物质浓度随时间变化如甲图所示[其中t0-t1阶段c(B)未画出]。t2时刻后改变条件反应体系中反应速率随时间变化的情况如乙图所示,且四个阶段都各改变一种条件并且改变的条件均不相同。下列说法正确的是()
 A.反应的方程式为3A(g)+B(g) 2C(g)
A.反应的方程式为3A(g)+B(g) 2C(g)
B.t3~t4,t4~t5,t5~t6各阶段可能改变的条件依次为:加催化剂,降低反应温度,增大压强
C.B的起始物质的量为0.08 mol
D.若t1="10" s,A在t0~t1时间段的反应速率为0.00225 mol·L-1·s-1
如图,C、D、E、F、X、Y都是惰性电极。将电源接通后,向(乙)中滴入酚酞溶液,在F极附近显红色.则下列说法正确的是()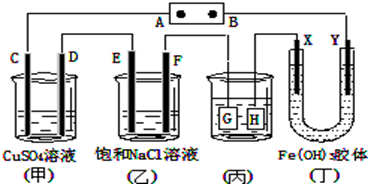
A.若用乙烷、空气燃料电池作电源,电解质为KOH溶液,则A极的电极反应式为:C2H6 -14e-+ 18OH-= 2CO32- + 12H2O
B.欲用(丙)装置给铜镀银,H应该是Ag,电镀液选是AgNO3溶液
C.(丁)装置中Y极附近红褐色变深,说明氢氧化铁胶体带正电荷
D.C、D、E、F电极均有单质生成,且其物质的量比为1:2:2:2