(10分) (1)北京奥运会“祥云”火炬燃料是丙烷(C3H8),亚特兰大奥运会火炬燃料是丙烯(C3H6)。
①丙烷脱氢可得丙烯。已知:C3H8(g)→CH4(g)+HC≡CH(g)+H2(g) △H1=+156.6 kJ·mol-1
CH3CH=CH2(g)→CH4(g)+HC≡CH(g) △H2=+32.4 kJ·mol-1
则相同条件下,反应C3H8(g)→CH3CH=CH2 (g)+H2(g)的△H= kJ·mol-1。
②以丙烷为燃料制作新型燃料电池,电池的正极通入O2和CO2,负极通入丙烷,电解质是熔融碳酸盐。电池反应总方程式为
;放电时CO32-移向电池的 (填“正”或“负”)极。
(2) 反应A(g)+B(g)
反应A(g)+B(g)  C(g)+D(g)过程中的能量变化如图所示,回答下列问题。
C(g)+D(g)过程中的能量变化如图所示,回答下列问题。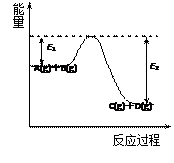
①该反应是_______________反应(填“吸热”“放热” );
②在反应体系中加入催化剂,反应速率增大,E1和E2的变化是:E1_________,E2________(填“增大”“减小”“不变” );
③反应体系中加入催化剂对反应热是否有影响?_____________,原因是______________________________________________________________________。
如图所示,试管中集满干燥的氯气,胶头滴管中装有供反应的足量浓氨水.滴入浓氨水,开始时试管内发生的反应有氧化还原反应:NH3+Cl2→N2+HCl并产生红光和白烟。
请根据以上反应和现象回答下列问题:
(1)标志反应全部完成的现象是______.
(2)反应完毕后,将试管浸入水中并倒立着试管,取下滴管,有水进入试管,在室温时,进入试管内的水约占试管容积的______。
(3)反应中生成的白烟是______。
(4)用写出试管中反应的化学方程式________。
实验室用氨气还原氧化铜的方法测定铜的近似相对原子质量,反应的化学方程式为: 2NH3+3CuO
 N2+3Cu+3H2O
N2+3Cu+3H2O
试回答:(1)如果选用测定反应物CuO和生成物H2O的质量[m(CuO)、m(H2O)]时,请用下列仪器设计一个简单的实验方案。
①仪器连接的顺序(用字母编号表示,仪器可重复使用);d中浓硫酸的作用是,;实验完毕时观察到a中的现象是;
②列出计算Cu的相对原子质量的表达式;
③下列情况将使测定结果偏大的是。(以下选择填空不限1个正确答案,均用字母编号填写)
(a)CuO未全部还原为Cu (b)CuO受潮 (c)CuO中混有Cu
(2)如果仍采用上述仪器装置,其他方案可选用测定的物理量有
(a)m(Cu)和m(CuO) (b)m(N2)和m(H2O) (c)m(Cu)和m(H2O) (d)m(NH3)和m(H2O)
质检总局通报全国婴幼儿奶粉三聚氰胺含量抽检结果,伊利、蒙牛、圣元、雅士利等22个厂家69批次产品中检出三聚氰胺,并被要求立即下架。乳制品的蛋白氮的测定是质检部门的一个常见的工作。实验室常利用甲醛法测定(NH4)2SO4样品中氮的质量分数,其反应原理为: 4NH4+ +6HCHO =3H++6H2O+(CH2)6N4H+ [滴定时,1 mol (CH2)6N4H+与 l mol H+相当],然后用NaOH标准溶液滴定反应生成的酸。某兴趣小组用甲醛法进行了如下实验: 步骤I称取样品1.500 g。
步骤I称取样品1.500 g。 步骤II将样品溶解后,完全转移到250 mL容量瓶中,定容,充分摇匀。
步骤II将样品溶解后,完全转移到250 mL容量瓶中,定容,充分摇匀。 步骤III移取25.00 mL样品溶液于250 mL锥形瓶中,加入10 mL 20%的中性甲醛溶液,摇匀、静置5 min后,加入1~2滴酚酞试液,用NaOH标准溶液滴定至终点。按上述操作方法再重复2次。
步骤III移取25.00 mL样品溶液于250 mL锥形瓶中,加入10 mL 20%的中性甲醛溶液,摇匀、静置5 min后,加入1~2滴酚酞试液,用NaOH标准溶液滴定至终点。按上述操作方法再重复2次。 ⑴根据步骤III填空:
⑴根据步骤III填空: ①碱式滴定管用蒸馏水洗涤后,直接加入NaOH标准溶液进行滴定,则测得样品中氮的质量分数________(填“偏高”、“偏低”或“无影响”)。
①碱式滴定管用蒸馏水洗涤后,直接加入NaOH标准溶液进行滴定,则测得样品中氮的质量分数________(填“偏高”、“偏低”或“无影响”)。 ②锥形瓶用蒸馏水洗涤后,水未倒尽,则滴定时用去NaOH标准溶液的体积__________(填“偏大”、“偏小”或“无影响”)
②锥形瓶用蒸馏水洗涤后,水未倒尽,则滴定时用去NaOH标准溶液的体积__________(填“偏大”、“偏小”或“无影响”) ③滴定时边滴边摇动锥形瓶,眼睛应观察____________
③滴定时边滴边摇动锥形瓶,眼睛应观察____________ A.滴定管内液面的变化 B.锥形瓶内溶液颜色的变化
A.滴定管内液面的变化 B.锥形瓶内溶液颜色的变化 ④滴定达到终点时,酚酞指示剂由_________色变成_________色。
④滴定达到终点时,酚酞指示剂由_________色变成_________色。 ⑵滴定结果如下表所示:
⑵滴定结果如下表所示:
滴定 次数 次数 |
待测溶液的体积 /mL /mL |
标准溶液的体积/mL |
|
| 滴定前刻度 |
滴定后刻度 |
||
| 1 |
25.00 |
1.02 |
21.03 |
| 2 |
25.00 |
2.00 |
21.99 |
| 3 |
25.00 |
0.20 |
20.20 |
若NaOH标准溶液的浓度为0.1010 mol·L-1,则该样品中氮的质量分数为___________。
中国人向来喜欢吉利,如第29届奥运会开幕定在——2008年8月8日8时。在有机化学中就有这样一个“吉利分子C8H8O8”,它与08年的奥运会同样有着引人注目的数字特征。已知:①X的相对分子质量小于180,其中氧的质量分数约为49.4%②1molX在稀硫酸中发生水解反应生成2mol甲醇和1molA③X中没有支链。根据以上信息填写下列空白: (1)1个X分子中,可能含有 个氧原子,X不可以发生的反应有 (填序号)
(1)1个X分子中,可能含有 个氧原子,X不可以发生的反应有 (填序号) ①加成反应 ②酯化反应 ③氧化反应 ④消去反应
①加成反应 ②酯化反应 ③氧化反应 ④消去反应 已知A物质能发生如图转化关系,E为高分子化合物,B为环状结构。回答下列问题
已知A物质能发生如图转化关系,E为高分子化合物,B为环状结构。回答下列问题
 (2)写出①的反应类型_____________,
(2)写出①的反应类型_____________, (3)写出④的化学方程式__________________________________________。
(3)写出④的化学方程式__________________________________________。 (4)B的组成结构很有特点,写出符合条件的有机物B有种结构,写出其中的含一个六元环的有机物B结构简式____________。
(4)B的组成结构很有特点,写出符合条件的有机物B有种结构,写出其中的含一个六元环的有机物B结构简式____________。 (5)一定量的A物质与乙醇的混合物完全燃烧生成27g水和V LCO2(标准状况),则等物质的量该混合物完全燃烧消耗氧气的物质的量为___________________。
(5)一定量的A物质与乙醇的混合物完全燃烧生成27g水和V LCO2(标准状况),则等物质的量该混合物完全燃烧消耗氧气的物质的量为___________________。
下图表示物质A~H的转化关系,其中D为非金属固体单质,其余的为化合物。①为工业生产中常见反应,且F必须密封保存,否则遇潮湿空气即产生含碳质量分数最高的常见气态烃。经测定固体G由三种元素组成,其中钙元素占50.00%、碳占15.00%(元素质量分数)。H是能使湿润的红色石蕊试纸变蓝的气体。

 ⑴F的电子式为
⑴F的电子式为 (2)写出③化学反应方程式
(2)写出③化学反应方程式 写出④化学反应方程式
写出④化学反应方程式 (3)B和H在一定的条件下反应可得到一种有机肥料甲。甲在一定条件下分解得到B、H和三聚氰胺(C3H6N6),请写出该反应方程式
(3)B和H在一定的条件下反应可得到一种有机肥料甲。甲在一定条件下分解得到B、H和三聚氰胺(C3H6N6),请写出该反应方程式