今有如下三个热化学方程式:
H2(g)+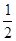 O 2(g)==H2O(g) ΔH="a" kJ·mol-1;
O 2(g)==H2O(g) ΔH="a" kJ·mol-1;
H2(g)+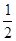 O 2(g)==H2O(l) ΔH="b" kJ·mol-1;
O 2(g)==H2O(l) ΔH="b" kJ·mol-1;
2H2(g)+O2(g)====2H2 O(l) ΔH="c" kJ·mol-1。
关于它们的下列表述正确的是
| A.a<b | B.a、b、c均为正值 | C.a=b | D.2b=c |
下列物质的熔点均按由高到低的次序排列,其原因是由于键能由大到小排列的是
| A.钠、干冰 | B.金刚石、晶体硅 |
| C.碘化氢、溴化氢 | D.二氧化硅、二氧化碳 |
A元素原子得电子变成阴离子释放出的能量比B元素原子得电子变成阴离子释放出的能量大,则
| A.氧化性A->B- | B.还原性 A->B- | C.氧化性 A>B | D.还原性A>B |
短周期元素Q、R、T、W在元素周期表中的位置如右图所示,其中T所处的周期序数与主族序数相等,下列说法正确的是
| A.W在周期表中的位置是第三周期ⅤA族 |
| B.原子半径Q>R>T |
| C.W原子得电子能力强于Q原子,且可形成共价化合物QW2 |
| D.原子序数比R多1的元素只能形成一种氢化物 |
以下物理量只与温度有关的是
| A.合成氨工业中,氢气的转化率 | B.醋酸钠的水解程度 |
| C.水的离子积 | D.氢气的溶解度 |
下列关于二氧化硅晶体的描述错误的是
| A.分子式为SiO2 | B.熔化时共价键断裂 |
| C.属于酸性氧化物 | D.1mol SiO2中含有4 mol Si-O键 |