某课外实验小组设计的下列实验合理的是( )
 |
 |
 |
 |
| A.制备少量氨气 |
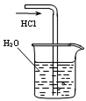
B.吸收HCl制取稀盐酸 |
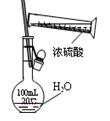
C.配制一定浓度硫酸溶液 |
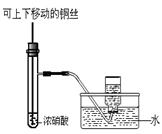
 C.制备并收集少量NO2气体 C.制备并收集少量NO2气体 |
科研、生产和生活中的下列做法,利用了氧化还原反应的是
| A.用乙醚从黄花蒿中提取青蒿素 |
| B.用氯化铁溶液腐蚀铜制印刷电路板 |
| C.在空气净化器中装入活性炭层 |
| D.服用阿司匹林出现水杨酸反应时用小苏打解毒 |
向5mLNaCl溶液中滴入一滴AgNO3溶液,出现白色沉淀,继续滴加一滴KI溶液并振荡,沉淀变为淡黄色,再滴加一滴Na2S溶液并振荡,沉淀又变为黑色,根据上述变化过程,分析此三种沉淀物的溶解度关系是()
| A.AgCl=AgI=Ag2S | B.AgI> AgCl> Ag2S |
| C.AgCl>AgI>Ag2S | D.AgCl<AgI<Ag2S |
将0.1mol/L的AlCl3溶液加热、蒸干、灼烧最后得到的固体是()
| A.Al | B.Al(OH)3 | C.AlCl3 | D.Al2O3 |
物质的量浓度相等的下列溶液pH值由大到小的顺序是()
| A.Na2CO3、NaHCO3、NaCl、NH4Cl |
| B.Na2CO3、NaHCO3、NH4Cl、NaCl |
| C.Na2CO3、NaCl、NH4Cl、NaHCO3 |
| D.Na2CO3、NH4Cl、NaHCO3、NaCl |
为了配制NH4+的浓度与Cl-的浓度比为1:1的溶液,可在NH4Cl溶液中加入适量()
①浓盐酸②NaCl固体③浓氨水④ NaOH固体
| A.①② | B.③ | C.③④ | D.④ |