分别称取0.2gNaOH固体两份,加适量的蒸馏水溶解,用未知浓度的盐酸滴定,若两次所消耗盐酸的体积分别为25.02mL、24.98mL,下列说法中正确的是
A.若盐酸的浓度为0.2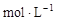 ,则第一次测出的盐酸的浓度偏高 ,则第一次测出的盐酸的浓度偏高 |
| B.若NaOH中混有少量的Na2CO3,则测定的结果偏高 |
| C.开始读数时仰视滴定管读数,滴定结束时也仰视滴定管读数,对实验结果无影响 |
| D.第二次测定的数据可能是由于滴定时不小心把盐酸滴到锥形瓶外面引起的 |
下列有关化学用语的表示正确的是
A.甲烷分子的球棍模型: |
| B.HClO的结构式:H-Cl-O |
C.质子数为53,中子数为78的碘原子: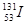 |
D.熔融状态下硫酸氢钾的电离方程式:KHSO4  K++H++SO42- K++H++SO42- |
亚氯酸钠是一种高效氧化剂漂白剂,主要用于棉纺、亚麻、纸浆等漂白。亚氯酸钠(NaClO2)在溶液中可生成ClO2、HClO2、ClO2-、Cl- 等,其中HClO2和ClO2都具有漂白作用,但ClO2是有毒气体。经测定,25℃时各组分含量随pH变化情况如图所示(Cl-没有画出)。则下列分析正确的是()
| A.亚氯酸钠在酸性条件下较稳定 |
| B.25℃时,HClO2的电离平衡常数的数值Ka=10-6 |
| C.pH越大,该漂白剂的漂白性能越好 |
| D.25℃,PH=3时,NaClO2溶液中:c(Na+)+ c(H+)=c(ClO2-)+ c(OH-) |
以酸性氢氧燃料电池为电源进行电解的实验装置如下图。下列叙述正确的是()
| A.燃料电池工作时,正极反应为O2+2H2O+4e-=4OH- |
| B.a极是铁,b极是铜时,b极逐渐溶解,a极上有铜析出 |
| C.a、b两极若是石墨,在相同条件下a极产生的气体与电池中消耗的H2体积相等 |
| D.a极是粗铜,b极是纯铜时,a极逐渐溶解,b极上有铜析出 |
部分短周期元素的有关信息为:
| 元素代号 |
元素性质或原子结构 |
| T |
第二层上的电子数是第一层的3倍 |
| R |
与T 同一族 |
| L |
L2+与T2-的核外电子数相等 |
| Q |
与L同族 |
| Z |
元素最高正价是+3价,与L同周期 |
根据上表中信息,判断以下叙述正确的是()
A.氢化物的稳定性为H2T<H2R
B.单质与稀盐酸反应的速率为L<Q
C.Z与T形成的化合物具有两性
D.L与R通过离子键形成的化合物阴阳离子的核外电子数相等
85岁中国女药学家屠呦呦因创制新型抗疟药青蒿素和双氢青蒿素而获得2015年诺贝尔生理学医学奖。颁奖理由是“因为发现青蒿素——一种用于治疗疟疾的药物,挽救了全球特别是发展中国家数百万人的生命。”下列关于青蒿素和双氢青蒿素(结构如图)说法错误的是()
| A.青蒿素和双氢青蒿素互为同分异构体 |
| B.青蒿素和双氢青蒿素均能发生取代反应 |
| C.青蒿素的分子式为C15H22O5 |
| D.青蒿素在一定条件下能与NaOH溶液反应 |