某澄清溶液,可能含有NH4+ 、Na+、K+、Cl-、CO32-、SO42-中的一种或几种,现做如下实验:
、Na+、K+、Cl-、CO32-、SO42-中的一种或几种,现做如下实验:
①取少量该溶液加入BaC l2溶液有白色沉淀生成,再加入足量盐酸后,沉淀部分溶解,并有气体生成。
l2溶液有白色沉淀生成,再加入足量盐酸后,沉淀部分溶解,并有气体生成。
②用铂丝蘸取少量该溶液置于无色酒精灯火焰中灼烧,火焰呈黄色,透过蓝色钴玻璃观察,未见紫色火焰。
③另取少量该溶液加入NaOH溶液并加热,将湿润的红色石蕊试纸靠近试管口无颜色变化。
(1)第①步可以检验出的离子是
(2)第②③步说明一定含有的离子是
(3)从以上操作中,不能判断是否存在的离子是 ,为了检验该离子是否存在,请你写出进一步检验的 操作步骤和实验现象:
操作步骤和实验现象:
实验室也可用KMnO4固体和浓盐酸反应制氯气,反应方程式如下:
2KMnO4+16HCl(浓)=2KCl+2MnCl2+8H2O+5Cl2↑
完成下列问题:
(1)该反应中氧化剂是,还原剂是,氧化产物是,还原产物是。
(2)用双线桥标出该反应的电子得失的方向和数目。
氢气、甲烷(CH4)、水各1g,其中含分子数最多的是;含氢原子最多的是;氢气、甲烷、水各1mol,含分子数是否一样多?(填“是”或“不是);含氢原子数最多的是。
今有九种物质:①铝②石墨③氯气④BaSO4晶体⑤纯硫酸⑥金刚石⑦石灰水⑧乙醇⑨熔化的KNO3(填序号)
其中能导电的是,属于电解质的是,既不是电解质,也不是非电解质的是。
根据下列微粒的结构示意图,写出相应的原子或离子符号: ,
,
已知2A(g)+B(g) 2C(g),向容积为1L的密闭容器中加入0.050mol A和0.025mol B,在500℃时充分反应,达平衡后测得
2C(g),向容积为1L的密闭容器中加入0.050mol A和0.025mol B,在500℃时充分反应,达平衡后测得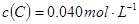 ,放出热量Q1 kJ。
,放出热量Q1 kJ。
(1)能说明上述反应已经达到化学平衡状态的是______________(填字母编号)
a.v(C)=2v(B)b.单位时间内生成2mol A的同时消耗1molB
c.容器内压强保持不变 d.容器内气体的密度保持不变
(2)若在相同的容器中只加入0.050mol C,500℃时充分反应达平衡后,吸收热量Q2 kJ,则Q1与Q2之间的关系式可表示为___________________________(用含Q1、Q2的代数式表示)。
(3)500℃时,上述反应的化学平衡常数K=____________________。
(4)已知K(300℃)>K(350℃),该反应是__________(填“放”或“吸”)热反应;若反应温度升高,A的转化率___________________(填“增大”、“减小”或“不变”)。
(5)某温度下,A的平衡转化率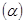 与体系总压强(P)的关系如图所示,平衡状态由a变到b时,化学平衡常数K(A)______________K(B)(填“>”、“<”或“=”)
与体系总压强(P)的关系如图所示,平衡状态由a变到b时,化学平衡常数K(A)______________K(B)(填“>”、“<”或“=”)