松油醇是一种调香香精,它是α、β、γ三种同分异构体组成的混合物,可由松节油分馏产品A(下式中的18是为区分两个羟基而人为加上去的)经下列反应制得: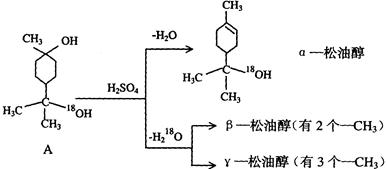
(1) α-松油醇的分子式 ;
α-松油醇的分子式 ;
(2)α-松油醇所属的有机物类别是 (多选扣分);
(a)醇 (b)酚 (c)饱和一元醇
(3)α-松油醇能发生的反应类型是 (多选扣分);
(a)加成 (b)水解 (c)氧化
(4)在许多香料中松油醇还有少量以酯的形式出现,写出RCOOH和α-松油醇反应的
化学方程式 (请注明18O所处的位置)
(请注明18O所处的位置)
(5)写结构简式:β松油醇
下列各组物质属于同系物的是,属于同分异物体的是;属于同素异形体的是,属于同一种物质的是。(填序号)
⑴O2和O3⑵氕和氚⑶麦芽糖和蔗糖⑷苯和对二甲苯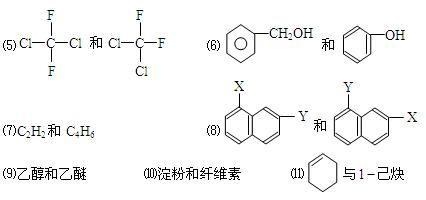
由CH3CH2Cl经过3步制乙二醇(HO CH2CH2OH,写出化学方程式,注明反应条件及反应类型:
(1)反应
(2)反应
(3)反应
现有A、B、C、D、E、F六种有机物,它们的转化关系如下图所示(图中部分反应条件及生成物没有全部写出)。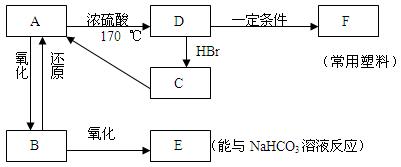
已知:溶液B能发生银镜反应,气体D是一种植物生长调节剂,其相对分子质量为28。
请回答下列问题:
(1)A、B、C的结构简式分别是、、;
(2)C → A反应的化学方程式是;
(3)D → F反应的化学方程式是;
(4)在一定条件下,A与E反应可生成一种具有香味的物质。该反应的化学方程式是
。
有A、B、C三种烃,它们的结构简式如下图所示: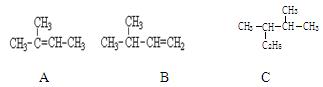
A的名称是;
B的名称是;
C的名称是。
(8分)按官能团的不同,可以对有机物进行分类,请指出下列有机物的种类,填在横线上。
CH3CH2CH2COOH __________;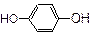 ___________;
___________;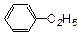 ___________;
___________; ___________;
___________; ___________;
___________;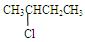 __________;
__________;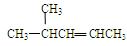 _____ ______;
_____ ______;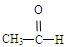 ;
;