向某晶体的水溶液中加入Fe2+的溶液后,无明显变化,当滴加几滴氯水后,混合液出现血红色。那么,由此得出下列的结论正确的是
| A.该晶体中没有SCN- | B.Fe3+的氧化性比Cl2的氧化性强 |
| C.Fe2+被Cl2氧化为Fe3+ | D.Fe2+与SCN-形成血红色的化合物 |
下列各组给定的物质中,每个原子最外层都满足8电子结构的是
| A.BF3 | B.SO2 | C.PCl3 | D.HClO |
下表为元素周期表前四周期的一部分,下列有关R、W、X、Y、Z五种元素的叙述中,正确的是
| A.X、Y、Z的阴离子电子层结构均与R原子的相同 |
| B.常压下,Y单质的沸点比Z单质的沸点高 |
| C.W的氢化物的稳定性比X的氢化物的稳定性强 |
| D.最高价氧化物的水化物酸性W比Y强 |
能说明苯分子中碳碳键不是单、双键相间交替的事实是
①苯不能使酸性KMnO4溶液褪色②苯环中碳碳键均相同
③邻二甲苯只有一种④苯的对位二元取代物只有一种
⑤苯的邻位二氯代物只有一种⑥在一定条件下苯与H2发生加成反应生成环己
| A.①②③④⑤ | B.①②③⑤ |
| C.②③④⑤⑥ | D.①②④⑥ |
某单烯烃经氢化后得到的饱和烃是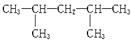 ,该烯烃可能有的结构有
,该烯烃可能有的结构有
| A.1种 | B.2种 | C.3种 | D.4种 |
运用元素周期律分析下面的推断,其中错误的是
①113号元素的单质是一种金属,它的氧化物的水化物不能与强碱反应;②砹(At2)是一种有色固体,HAt很不稳定,AgAt是有色难溶于水的固体;③硫酸锶是难溶于水和盐酸的固体;④H2S比水的还原性弱,但H2S比水的稳定性强;⑤周期表中钠在钾的上方,因此非金属性钠比钾弱,单质的熔点钠也比钾低;⑥第二周期非金属元素(除稀有气体元素)原子半径小,得电子能力强,其气态氢化物的水溶液均呈酸性
| A.③④⑤⑥ | B.④⑤⑥ | C.②③④ | D.③④⑥ |