(16分)给出下列氧化还原反应,试回答下列问题。
(1) KMnO4+ KI+ H2SO4 K2SO4+ MnSO4 + I2十 H2O
配平化学反应方程式
被还原的元素 ,发生氧化反应的物质 。 (2) 3Cl2 + 6NaOH 5NaCl + NaClO3 + 3H2O
(2) 3Cl2 + 6NaOH 5NaCl + NaClO3 + 3H2O
用双线桥标出电子转移的方向和数目 
氧化剂与还原剂的物质的量之比为 ,氧化产物是 。
(3)11P+15CuSO4+24H2O=6H3PO4+15H2SO4+5Cu3P(反应中Cu3P中的P为负三价)。
该反应中Cu2+表现 性(填氧化或还原);11molP中被P氧化的P是 mol
某些化学键的键能如下表所示(kJ·mol-1):
| 键 |
H-H |
Br-Br |
I-I |
Cl-Cl |
H-Cl |
H-I |
H-Br |
| 键能 |
436 |
193 |
151 |
247 |
431 |
299 |
356 |
(1)把1mol Cl2分解为气态原子时,需要_______(填“吸收”或“放出”) ________能量
(2)1mol H2在2mol Cl2中燃烧,放出的热量_______KJ。
(3)由表中所列化学键形成的单质分子中,最稳定的是________,最不稳定的是________,形成的化合物分子中,最稳定的是__________,最不稳定的是__________.
(4)在一定条件下,1mol H2与足量的Cl2、Br2、I2分别反应,放出热量由多到少的是____。
A.Cl2 > Br2 > I2 B.I2 > Br2 > Cl2
(5)预测1mol H2在足量F2中燃烧比在Cl2中放热。
(6)在液态HCl、HBr、HI中沸点最高的是。
A为常见烃是一种水果催熟剂,乙酸苯甲酯可提高花或果的芳香气味,常用于化妆品工业和食品工业。下图是乙酸苯甲酯的一种合成路线(部分反应物、产物和反应条件略去)。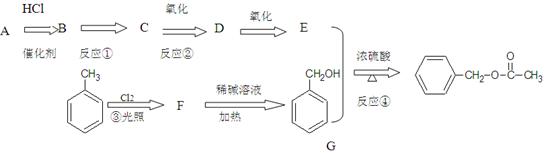
请回答:
(1)E的官能团名称为F的结构简式为
(2)反应①条件为,反应④的类型是
(3)反应②的化学方程式为;反应类型是
(4)物质D与新制氢氧化铜反应方程式为
(5)G有多种同分异构体,其中属于芳香族化合物的有种(不包括G)
写出其中的任意一种同分异构体的结构简式
回答下列问题:
① CH2=CH-CH=CH2 键线式__________②羟基(-OH)的电子式_____________
③ 的结构简式___________④芳香烃萘
的结构简式___________④芳香烃萘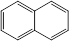 的分子式为
的分子式为
质量都是50 g的 HCl、NH3、CO2、O2四种气体中,含有分子数目最少的是_,含有原子数目最多的是,在相同温度和相同压强条件下,体积最大的是。
为了除去NaCl溶液中少量的MgCl2、Na2SO4,从稀盐酸,Na2CO3,K2CO3,Ba(NO3)2,Ba(OH)2溶液中,选择A、B、C 3种试剂,按图中步骤进行操作:
(1)下列试剂的化学式AC
(2)加入过量A的原因是,有关反应的离子方程式是,
(3)加入过量B有关反应的离子方程式是。