乙炔是有机合成工业的一种原料。工业上常用CaC2与水反应生成乙炔。
(1)CaC2中的C22-与O2 2+、N2互为等电子体,N2的结构式为 O22+的电子式可表示为 ;1mol O22+中含有的π键数目为
2+、N2互为等电子体,N2的结构式为 O22+的电子式可表示为 ;1mol O22+中含有的π键数目为
(2)将乙炔通入[Cu(NH3)2]Cl溶液生成Cu2C2红棕色沉淀。Cu+基态核外电子排布式为
(3)乙炔与氢氰酸反应可得丙烯腈(H2C=CH-C=N). 丙烯腈分子中所有碳原子轨道杂化类型为 ;分子中处于同一直线上的原子数目最多为 。
1L某烃的蒸气完全燃烧生成的CO2比水蒸汽少1L(同温同压下测定);0.1mol该烃完全燃烧后的产物被碱石灰充分吸收,碱石灰增重39g。求:
(1)该烃的分子式。
(2)若该烃的一氯代物有三种,写出该烃所有可能的结构简式和名称。
随着经济的不断发展,人们对环境问题也越来越关注。
(1)室内空气污染问题得到越来越多的关注,下列物质中也属于室内挥发性有机污染物的是
___________________。(填字母)
a.苯 b.甲烷 c.醋酸 d.乙烯
(2)下列措施中,有利于降低室内污染物浓度的是__________。(填字母)
a.勤开窗通风 b.日常生活中利用天然气替代煤作燃料
c.使用“绿色环保”装饰材料 d.室内放一些活性碳
(3) “温室效应”是全球关注的环境问题之一。CO2是目前大气中含量最高的一种温室气体。因此,控制和治理CO2是解决温室效应的有效途径。将CO2转化成有机物可有效实现碳循环。CO2转化成有机物的例子很多,如:
a.6CO2 + 6H2O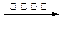 C6H12O6+6O2 b.CO2 + 3H2
C6H12O6+6O2 b.CO2 + 3H2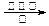 CH3OH +H2O
CH3OH +H2O
c.CO2 + CH4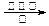 CH3COOHd.2CO2 + 6H2
CH3COOHd.2CO2 + 6H2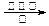 CH2==CH2 + 4H2O
CH2==CH2 + 4H2O
以上反应中,最节能的是,原子利用率(原子利用率=期望产物的总质量与生成物的总质量之比)最高的是。
(4) “汽车尾气污染”已倍受世人关注。以辛烷(C8H8)代表汽油的成分,要使辛烷正好完全燃烧,则辛烷气与空气(空气中O2占1/5体积)的体积比(相同条件下)为(保留三位小数)。
下图是CH2=CH—CH=CH2合成D(OHC—CH=CH—CHO)的流程。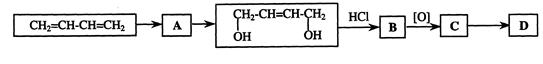 回答下列问题:
回答下列问题:
(1)若A为溴代物写出其结构简式。
(2)写出B C反应的化学方程式。
C反应的化学方程式。
(3)写出C D的反应类型。
D的反应类型。
(4)已知CH2=CH—CH=CH2+CH2=CH2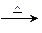
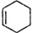 ,请写出CH2=CH—CH=CH2两分子加成后的产物。
,请写出CH2=CH—CH=CH2两分子加成后的产物。
某含苯环的化合物A,其相对分子质量为104,碳的质量分数为92.3%。
(1)A的分子式为。
(2)A与溴的四氯化碳溶液反应的化学方程式为,反应类型是;
(3)已知: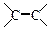

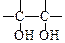 。请写出A与稀、冷的KMnO4溶液在碱性条件下反应所得的产物;
。请写出A与稀、冷的KMnO4溶液在碱性条件下反应所得的产物;
(4)一定条件下,A与氢气反应,得到的化合物中碳的质量分数为85.7%,写出此化合物的结构简式;
(5)在一定条件下,由A聚合得到的高分子化合物的结构简式为。
已知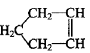 可简写为
可简写为
I.降冰片烯的分子结构可表示为: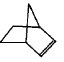
(1) 降冰片烯属于__________。
a. 环烷烃 b. 不饱和烃 c. 烷烃 d. 芳香烃
(2)降冰片烯不具有的性质__________。
a. 能溶于水 b. 能发生氧化反应
c. 能发生加成反应 d. 常温常压下为气体
II.利用某些有机物之间的相互转换可以贮存太阳能,如原降冰片二烯(NBD)经过太阳光照转化成为四环烷(Q)的反应为
(1)NBD有多种同分异构体,其中属芳香烃的只有一种,其结构简式为,系统命名为。
(2) 四环烷(Q)一氯代物共有种。