下列装置或操作能达到实验目的的 ( )
在醋酸溶液中,CH3COOH的电离达到平衡的标志是
| A.溶液显电中性 |
| B.溶液中无醋酸分子 |
| C.氢离子浓度恒定不变 |
| D.溶液中CH3COOH和CH3COO-共存 |
下列叙述中,能证明某物质是弱电解质的是
| A.熔融时不导电 |
| B.水溶液的导电能力很差 |
| C.不是离子化合物,而是极性共价化合物 |
| D.溶液中已电离的离子和未电离的分子共存 |
以铬酸钾为原料,电化学法制备重铬酸钾的实验装置示意图如下: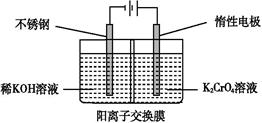
下列说法不正确的是
A.在阴极室,发生的电极反应为:2H2O+2e- 2OH-+H2↑ 2OH-+H2↑ |
B.在阳极室,通电后溶液逐渐由黄色变为橙色,是因为阳极区H+浓度增大,使平衡2CrO42-+2H+ Cr2O72-+H2O向右移动 Cr2O72-+H2O向右移动 |
C.该制备过程中总反应的化学方程式为4K2CrO4+4H2O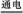 2K2Cr2O7+4KOH+2H2↑+O2↑ 2K2Cr2O7+4KOH+2H2↑+O2↑ |
D.测定阳极液中K和Cr的含量,若K与Cr的物质的量之比(nK/nCr)为d,则此时铬酸钾的转化率为1-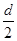 |
MgAgCl电池是一种能被海水激活的一次性贮备电池,电池反应方程式为
2AgCl+ Mg === Mg2++ 2Ag +2Cl-。有关该电池的说法正确的是
| A.Mg为电池的正极 |
| B.负极反应为AgCl+e-===Ag+Cl- |
| C.不能被KCl 溶液激活 |
| D.可用于海上应急照明供电 |
下列有关说法正确的是
| A.若在海轮外壳上附着一些铜块,则可以减缓海轮外壳的腐蚀 |
| B.2NO(g)+2CO(g)===N2(g)+2CO2(g)在常温下能自发进行,则该反应的ΔH>0 |
| C.用锡焊接的铁质器件,焊接处易生锈 |
| D.对于乙酸与乙醇的酯化反应(ΔH<0),加入少量浓硫酸并加热,该反应的反应速率和平衡常数均增大 |