下列说法,你认为不正确的是( )。
| A.平衡常数随温度的改变而改变 |
B.对于密闭容器中反应2SO2+O2 2SO3,2体积SO2与足量O2反应,能生成2体积SO3 2SO3,2体积SO2与足量O2反应,能生成2体积SO3 |
| C.合成氨反应中使用催化剂,降低了反应所需要的活化能。 |
D.反应H2(g)+I2(g)  2HI(g) 在450℃时,其平衡常数为49;则反应 2HI(g) 在450℃时,其平衡常数为49;则反应 |
HI(g)  1 ∕ 2 H2(g) +1 ∕ 2 I2(g) 在450℃时的平衡常数为1 ∕ 7
1 ∕ 2 H2(g) +1 ∕ 2 I2(g) 在450℃时的平衡常数为1 ∕ 7
在体积相同的两个密闭容器中分别充满O2、O3气体,当这两个容器内温度和气体密度相等时,下列说法正确的是
| A.两种气体的压强相等 | B.O2比O3质量小 |
| C.两种气体的分子数目相等 | D.两种气体的氧原子数目相等 |
类比归纳是学习化学的重要方法,对如F类比的说法正确的是
| A.CO2、SO2部是酸性氧化物,都能使酸性高锰酸钾溶液褪色 |
| B.MgO、Al2O3都是高熔点离子化合物,熔化时都能导电 |
| C.CO2与SiO2都是第IV A族的最高氧化物,则它们的物理性质也相似 |
| D.Al2O3与Fe2O3化学式相似,都是不溶于水的碱性氧化物 |
下列说法正确的是
| A.离子化合物中一定含有金属元素 | B.构成分子晶体的微粒中一定含有共价键 |
| C.原子晶体熔化要破坏共价键 | D.只有离子化合物中才存在离子 |
下列有关化学用语使用正确的是
A.NH4Br的电子式: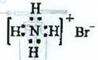 |
B.S2-的结构示意图: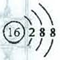 |
| C.乙酸的分子式:CH3COOH |
D.原子核内有18个中子的氯原子: |
下列物质与其用途相符合的是
①Cl2一做消毒剂②AgBr—制胶卷,感光纸③NaClO—漂白纺织物
④SO2—作防腐荆⑤淀粉一检验I2的存在⑥HOCH2CH2OH—抗冻剂
| A.②③④⑤⑥ | B.①②③④⑤ | C.①②③⑤ | D.全部 |