(10分) 根据下列框图回答问题(答题时,方程式中的M、E用所对应的元素符号表示):

⑴写出M溶于稀H2SO4和H2O2混合液的化学方程式: 。
⑵某同学取X的溶液,酸化后加入KI、淀粉溶液,变为蓝色。写出与上述变化过程相关的离子方程式: 、 。
⑶写出Cl2将Z氧化为K2EO4的化学方程式: 。
⑷由E制备的E(C2H5)2的结构如右图,其中氢原子的化学环境完全相同。但早期人们却错误地认为它的结构为: 。核磁共振法能够区分这两种结构。在核磁共振氢谱中,正确的结构有 种峰,错误的结构有 种峰。
。核磁共振法能够区分这两种结构。在核磁共振氢谱中,正确的结构有 种峰,错误的结构有 种峰。
Ⅰ、处于下列状态的物质中:①NaCl ②CO2 ③NH3·H2O④Cu ⑤HCl ⑥NaOH ⑦酒精 ⑧H2O ⑨NaCl溶液 ⑩NH3
(1)属于强电解质的是 (填序号,下同) ;
(2)属于弱电解质的是 ;
(3)属于非电解质的是 ;
Ⅱ、写出下列反应的离子方程式
(1)向澄清石灰水中加盐酸 ;
(2)用石灰石与盐酸反应制取二氧化碳 ;
(3)氢氧化钠溶液与氯化铵溶液混合后加热 ;
(1)对于可逆反应,升高温度,化学平衡向 热反应方向移动。
(2)对于有气体参加的可逆反应,增大压强,化学平衡向气体体积 (增大或小) 的方向移动。
(3)使用催化剂,能同等程度的改变正逆化学反应速率,化学平衡
(4)氢气的燃烧热为285.8千焦,其热化学方程式为:
(5)甲溶液的pH是4,乙溶液的pH是5,甲溶液与乙溶液的c(H+))之比:
在密闭容器中进行反应①Fe(s)+CO2(g)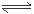 FeO(s)+CO(g)ΔH1=akJ·mol一1
FeO(s)+CO(g)ΔH1=akJ·mol一1
反应②2CO(g)+O2(g)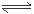 2CO2(g)△H2="b" kJ·mol-1
2CO2(g)△H2="b" kJ·mol-1
反应③2Fe(s)+O2(g)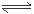 2FeO(s) △H3
2FeO(s) △H3
(1) △H3= (用含a、b的代数式表示)。
(2)反应①的化学平衡常数表达式K= ,已知500℃时反应①的平衡常数K=1.0,在此温度下2 L密闭容器中进行反应①,Fe和CO2的起始量均为2.0 mol,达到平衡时CO2的转化率为 ,CO的平衡浓度为 。
(3)将上述平衡体系升温至700℃,再次达到平衡时体系中CO的浓度是CO2浓度的两倍,则a 0(填“>”、“<”或“=”)。为了加快化学反应速率且使体系中CO的物质的量增加,其他条件不变时,可以采取的措施有 (填序号)。
| A.缩小容器的体积 | B.再通入CO2 |
| C.升高温度 | D.使用合适的催化剂 |
(4)下列图像符合反应①的是 (填序号)(图中V是速率、φ为混合物中CO含量,T为温度)。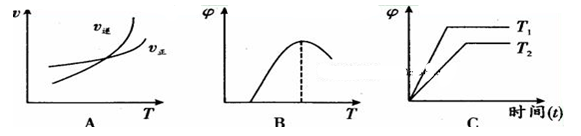
在一定体积的密闭容器中,进行如下化学反应:CO2(g)+H2(g)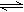 CO(g)+H2O(g),其化学平衡常数K和温度t的关系如下表:
CO(g)+H2O(g),其化学平衡常数K和温度t的关系如下表:
| t℃ |
700 |
800 |
830 |
1000 |
1200 |
| K |
0.6 |
0.9 |
1.0 |
1.7 |
2.6 |
回答下列问题:
(1)该反应的化学平衡常数表达式为K=_____________
(2)该反应为_____________反应(选填“吸热”“放热”)。
(3)能判断该反应是否达到化学平衡状态的依据是_____________。
A.容器中压强不变 B.混合气体中c(CO)不变
C.v正(H2)=v逆(H2O) D.c(CO2) = c(CO)
(4)某温度下,平衡浓度符合c(CO2)·c(H2)= c(CO)﹒ c(H2O),试判断此时的温度为 ℃。
请把下列物质按类别填空:
A Na2O B K2SO4 C NaHCO3D镁铝合金
E Na F CaO G CaCO3 H Ca(OH)2
(1)属于盐的是________________________________;
(2)属于碱的是________________________________;
(3)属于单质的是________________________________;
(4)属于氧化物的是________________________________。