A是一种强酸,其浓度超过40%时就会迅速分解,产生比它的酸性更强的酸B,同时放出气体C和D,该气体经干燥后,平均分子量为47.6,所得气体通过80℃NaOH溶液,得到的产物中一种是A的钠盐,同时还剩余一种可以使带火星的木条复燃的气体D。试完成下列各题:
(1)确定各物质的化学式A________、B________、C________、D____________;
(2)气体C和D的体积比__________ _____;
_____;
(3)写出A分解方程式并配平; ;
(4)写出气体C与湿润的淀粉-碘化钾试纸的反应方程式_____________________;
(5)写出将气体C通过80℃NaOH溶液时发生的反应方程式___________________。
(每空2分,共16分).下图中的A、B、C、D、E、F、G均为有机物
据上图回答问题:
(1)D的化学名称是。
(2)G与溴水反应的化学方程式是(有机物须用结构简式表示)。
(3)B的分子式是:A的结构简式是①反应的反应类型是。
(4)符合下列3个条件的B的同分异构体的数目有个
(ⅰ)含有邻二取代苯环结构
(ⅱ)与B有相同官能团
(ⅲ)不与FeCl3溶液发生显色反应。
写出其中任意一个同分异构体的结构简式。
(5)G是的工业原料,用化学方程式表示G的一种的工业用途。
(每空2分,共14分)已知苯甲醛在一定条件下可以通过Perkin反应生成肉桂酸(产率45%~50%),另一个产物A也呈酸性,反应方程式如下: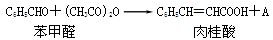
(1)Perkin反应合成肉桂酸的反应式中,反应物的物质的量之比为1:1,产物A的名称是。
(2)一定条件下,肉桂酸与乙醇反应生成香料肉桂酸乙酯,其反应方程式为。
(3)取代苯甲醛也能发生Perkin反应,相应产物的产率如下:
| 取代苯甲醛 |
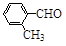 |
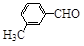 |
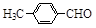 |
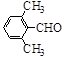 |
| 产率(%) |
15 |
23 |
33 |
0 |
| 取代苯甲醛 |
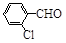 |
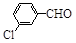 |
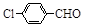 |
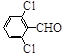 |
| 产率(%) |
71 |
63 |
52 |
82 |
可见,取代基对Perkin反应的影响有(写出3条即可):
①________________________________
②____________________
③________________________________
(4)溴苯(C6H5Br)与丙烯酸乙酯(CH2=CHCOOC2H5)在氯化钯(PbCl2)催化下可直接合成肉桂酸乙酯,该反应属于Beck反应,是芳香环上的一种取代反应,其反应方程式为____。
(5)Beck反应中的有机产物不能发生的反应是__________(填字母)。
(A)加成反应(B)取代反应(C)氧化反应(D)消去反应
(14分,每空2分)下图表示的反应关系中,部分产物被略去。已知2 mol白色固体粉末X受热分解,恢复到室温生成白色固体A、无色液体B、无色气体C各1 mol。X、E、G的焰色反应均为黄色。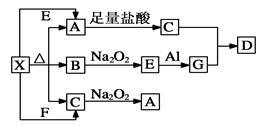
回答下列问题:
(1)写出下列物质的化学式:G______,D______。
(2)写出G与C反应生成D的化学反应方程式:____________________________。
(3)写出X+E→A的离子方程式:______________________________________。
(4)写出C与Na2O2参加反应的化学方程式:_____________________________。
0.2 mol Na2O2转移的电子数为________个。
(5)写出物质X的用途(至少写出一种)________。
(15分,每小题3分)某厂的酸性工业废水中含有一定量的Na+、Al3+、Fe3+、Cu2+、Cl-。该厂利用如图所示的工艺流程图,利用常见的气体氧化物、酸、碱和工业生产中的废铁屑,从废水中生产出了氯化铁、氧化铝、NaCl晶体和金属铜,产生了很好的社会经济效益。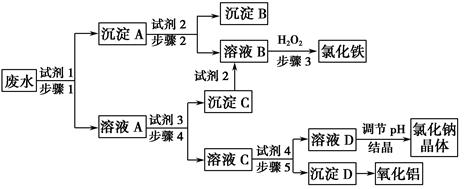
请填写下列空白:
(1)图中试剂1是____,试剂2是_____。
(2)步骤1和步骤2所用到的玻璃仪器是________。
(3)步骤1反应的离子方程式为____________________。
(4)步骤3反应的离子方程式为____________________。
(5)从节约药品和环保方面考虑,步骤5所发生反应的离子方程式应为____。
除去下列物质中所含有的杂质(括号内为杂质),将选用的试剂及分离方法填在题后的横线上,涉及化学反应的并写出有关反应的化学方程式(是离子反应的,写出其离子方程式)。
(1)Fe2O3[Fe(OH)3]________,__________________;
(2)FeCl3溶液(FeCl2)________,______________________;
(3)Fe(Al)___,_______________________。
(4)CO2(SO2),。
(5)SiO2(Al2O3),。
(6)淀粉溶液(氯化钠)。
(7)KNO3(NaCl)。
(8)Br2(H2O)。