(7分)某兴趣小组根据实验室提供的仪器和药品进行了氧气的制备实验。
(1)甲同学选用如右图所示的装置制取氧气。
①写出仪器A的名称: ▲ 。
②甲同学应选取的试剂是MnO2和 ▲ (填化学式),MnO2固体在该反应中起 ▲ 作用。
③除用排水法外,甲同学还可选择 ▲ 法收集氧气。
(2)乙同学称取一定质量KMnO4放在大试管中,将温度控制在250℃加热制取O2,该反
应的反应表达式为 ▲ (用化学式表示)。实验结束时,乙同学发现收集到的O2大于理论产量,针对这一现象,同学们进行了如下探究:
【提出猜想】猜想Ⅰ:反应生成的MnO2分解放出O2;
猜想Ⅱ:反应生成的K2MnO4分解放出O2
做出上述猜想的理由是 ▲ 。
【实验验证】同学们分为两组,分别进行以下实验:
①第一组同学取一定质量的MnO2,在250℃条件下加热一段时间,冷却后测得MnO2的质量不变。则猜想 ▲ 错误。
②第二组同学取K2MnO4置于试管中,在250℃条件下加热,没有用测定K2MnO4质量的方法,而是用了另一种实验方法得出了猜想Ⅱ是正确的。该组同学选择的实验方法是
▲ 。
化学兴趣小组的同学们探究用
从含
和
的溶液中获取金属
的原理.请你一起参与探究.
(1)实验依据:金属活动顺序.请在下表对应的方框内填入铁和铜的元素符号.
(2)意外发现:小明将光亮的铁丝插入含
和
的废液中,一段时间后取出,意外地发现铁丝表面没有变红.
(3)提出问题:
为什么没有从废液中置换出
?
(4)提出假设:小丽认为在铁丝表面可能有
析出,但被
溶液溶解了.
(5)验证假设:提供的主要实验用品:洁净的铁丝和铜丝各两根,相同体积、相同浓度的
溶液三份[
溶液显黄色].
| 实验操作 |
实验现象和数据 |
结论 |
| ①准确称量洁净的铁丝和铜丝的质量 |
铁丝质量为ag, 铜丝质量为bg |
\ |
| ②将铁丝插入
溶液中,一段时间后取出、洗净、干燥、称量 |
铁丝质量为mg,(m<a),溶液有黄色变为浅绿色 |
一定有生成(填化学式) |
| ③将铜丝插入
溶液中,一段时间后取出、洗净、干燥、称量 |
铜丝质量为ng(n<b) |
铜(填"能"或"不能")与
溶液反应 |
| ④另取相同质量、相同粗细的洁净铁丝和铜丝互相缠绕,插入
溶液中,一段时间后取出、洗净、干燥、分别称量铁丝和铜丝的质量 |
铁丝质量较轻 铜丝质量不变 |
Fe、
共存时优先与
溶液反应 |
(6)实验结论:小丽的假设(选填"成立"或"不成立"),理由是;
(7)思考与交流:
①兴趣小组的同学们通过对上述实验的分析,找到了用
从含
和
的溶液中提取金属
的关键,并且最终实验获得了成功,其实验成功的关键是:.并且反应充分.
②已知
和
发生化合反应.请按反应顺序写出用
从含
和
的溶液中获取金属
的化学方程式:;.
某化学兴趣小组的同学为了探究"复分解反应发生的条件",做了两个实验:
溶液分别与
溶液、
溶液反应.实验结束后将两实验中的废液倒入同一个干净的烧杯中,充分混合后过滤,得到滤液呈无色.
(1)写出废液混合后使滤液变无色时一定发生的反应的化学方程式:.
(2)取少量滤液于试管中,滴入紫色石蕊试液,石蕊溶液仍为紫色,则滤液呈性(填"酸"、"中"、"碱").
(3)该小组的同学对滤液中溶质的成分继续进行了如下探究实验:
【提出问题】滤液中溶质的成分是什么?
【作出猜想】猜想Ⅰ:;猜想Ⅱ;猜想Ⅲ.
【实验探究】
| 实验操作 |
实验现象 |
实验结论 |
| 实验①:取少量滤液于试管中,加入适量的纯碱溶液,振荡. |
无明显现象 |
猜想Ⅱ不成立 |
| 实验② |
产生白色沉淀 |
猜想Ⅲ成立 |
在实验②的溶液中滴加无色酚酞溶液,观察到酚酞溶液变成红色.
【交流拓展】要使蓝色溶液变成无色,还可以用不同于上述原理的方法,即在蓝色溶液中加入足量的.
探究(1):碳酸氢钠(
)俗名小苏打,常用于食品和医学工业.某化学兴趣小组的同学对碳酸氢钠进行加热,发现有气泡,同时还剩余白色固体.他们对白色固体进行探究.
【提出问题】这白色固体是什么?
【查阅资料】碳酸氢钠受热易分解生成水、二氧化碳和一种常见的固体.
【提出猜想】
猜想1:白色固体是碳酸钠,
猜想2:白色固体是氢氧化钠
猜想3:白色固体是氢氧化钠和碳酸钠的混合物
【实验探究】
兴趣小组为了确定反应后的固体产物成分,进行了如下实验,请填写下表:
| 实验方案 |
实验现象 |
结论 |
| 步骤一:取少量反应后的固体产物溶于水,加入过量的中性氯化钙溶液,过滤. |
产生白色沉淀 |
猜想1成立 |
| 步骤二:取滤液少许,往滤液中滴入:① | ② |
【实验总结】写出碳酸氢钠受热分解的化学方程式③.
探究2:某化学兴趣小组把金属钠投到硫酸铜溶液中,实验并非如想象的有红色铜析出,而是生成一种蓝色沉淀.同学们非常好奇并进行实验探究.
【提出问题】金属钠投到硫酸铜溶液中到底发生了怎样的化学反应?
【查阅资料】钠是非常活泼的金属,能与水发生剧烈反应,并放出气体,生成的溶液显碱性
【提出猜想】
猜想1:钠先与水反应生成氢气和某碱溶液,某碱再与硫酸铜反应生成蓝色沉淀;
猜想2:钠先与水反应生成某气体和某碱溶液,某碱再与硫酸铜反应生成蓝色沉淀;
【实验探究】
实验一:同学们把一小块切干净的钠投到装有少量蒸馏水的试管中,点燃生成的气体,听到"噗"的一声后燃烧起来;
实验二:在剩余的溶液中加入硫酸铜溶液,发现有蓝色沉淀.
【实验总结】
①两个猜想中的"某碱"是,猜想2中生成的气体是;
②水与金属钠反应的化学方程式.
③请你判断猜想成立.
根据下图回答下列问题: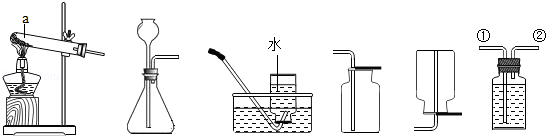
(1)仪器a的名称 .
(2)实验室用过氧化氢溶液和二氧化锰混合制取氧气,反应的化学方程式是 ;如果用F收集氧气,则气体由 进入 ( 填 ①或 ②).
(3)如果实验室要制取并收集二氧化碳气体,选择的装置连接是 (填字母).
和
溶液能发生反应,但看不到明显现象.某化学兴趣小组为验证CO2与NaOH溶液发生了反应,进行如下探究活动.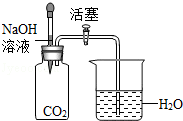
[查阅资料]
(1)
和
反应的化学方程式为.
[设计实验]
(2)方案一:
| 实验操作 |
实验现象 |
结论 |
| 往盛有
溶液的试管中通入
,然后滴入足量的 |
|
和
溶液发生了反应 |
(3)方案二:按如图所示装置进行实验.
| 实验操作 |
实验现象 |
结论 |
| . |
烧杯中的水吸入集气瓶中. |
和
溶液发生了反应 |
[反思与评价]
(4)有同学认为方案二根据实验现象不能得出"
和
溶液能发生反应"的结论,还应再做对比实验,理由是.