将a g铁和氧化铁的混合物加入足量的盐酸中充分反应后,固体无剩余,测得参加反应的HCl为0.08 mol,放出标准状况下的气体0.224 L。则下列判断中正确的是
| A.原混合物中n(Fe)∶n(Fe2O3)=2∶1 |
| B.向溶液中滴入KSCN溶液,显血红色 |
| C.无法计算原混合物的质量 |
D.此时溶液中Fe2+和Fe3+ 的物质的量之比为3∶1 的物质的量之比为3∶1 |
α1和α2分别为A在两个恒容容器中平衡体系A(g) 2B(g)和2A
2B(g)和2A (g) B(g)的转化率,在温度不变的情况下,均增加A的物质的量,下列判断正确的是()
(g) B(g)的转化率,在温度不变的情况下,均增加A的物质的量,下列判断正确的是()
| A.α1、α2均减小 | B.α1、α2均增大 |
| C.α1增大,α2减小 | D.α1减小,α2增大 |
下列说法不正确的是()
| A.一个反应能否自发进行取决于该反应放热还是吸热 |
| B.同一条件下不同物质有不同的熵值,其体系的混乱程度越大,熵值越大 |
| C.焓变是一个与反应能否自发进行有关的因素,多数能自发进行的反应都是放热反应 |
| D.一个反应能否自发进行,与焓变和熵变的共同影响有关 |
下图所示装置中,a、b都是惰性电极,通电一段时间后,a极附近溶液呈红色。下列说法正确的是()
| A.NaCl溶液浓度不变 | B.X是负极,Y是正极 |
| C.CuSO4溶液浓度变小 | D.X是正极,Y是负极 |

对于反应A2+3B2 2C来说,以下化学表示的反应速率最快的是()
2C来说,以下化学表示的反应速率最快的是()
A.v(B2)="0.8" mol·L-1·s-1 B. v(B2)="0.42" mol·L-1·s-1
C.v(C)="0.6" mol·L-1·s-1 D. v(A2)="0.4" mol·L-1·s-1
温度不变,在恒容的容器中进行下列反应:N2O4(g)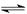 2NO2(g),若N2O4的浓度由0.1 mol· L-1降到0.07 mol· L-1需要15 s,那么N2O4的浓度由0.07 mol·L-1降到0.05 mol·L-1所需反应的时间()
2NO2(g),若N2O4的浓度由0.1 mol· L-1降到0.07 mol· L-1需要15 s,那么N2O4的浓度由0.07 mol·L-1降到0.05 mol·L-1所需反应的时间()
| A.大于10 s | B.等于10 s | C.等于5 s | D.小于10 s |