中和热的测定是高中重要的定量实验。取0.55 的NaOH溶液50mL与0.50
的NaOH溶液50mL与0.50 的盐酸50mL置于右图所示的装置中进行中和热的测定实验,回答下列问题:
的盐酸50mL置于右图所示的装置中进行中和热的测定实验,回答下列问题:
(1)从右图实验装置看,其中尚缺少的一种玻璃用品是____________,除此之外,装置中的一个明显错误是 。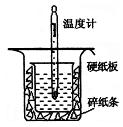
(2)右图中的小烧杯应该选择下列哪种规格的 。(选填代号)
①50 mL ②100 mL ③150 mL ④250 mL
(3)为了便于计算,假定混合前后溶液的密度都近似为1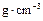 ,假定反应后生成溶液的比热容近似为水的比热容
,假定反应后生成溶液的比热容近似为水的比热容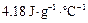 ,用t1℃和t2℃代表反应前后溶液的温度,则该实验中和热的计算表达式为
,用t1℃和t2℃代表反应前后溶液的温度,则该实验中和热的计算表达式为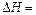 。
。
某化学实验小组的同学利用乙醇和浓硫酸制备乙烯气体并验证乙烯的某些化学性质。步骤如下:
①在一蒸馏烧瓶中加入约20mL乙醇和浓硫酸(体积比为1∶3),再加入少量的碎瓷片;
②瓶口插上带温度计的橡皮塞;
③加热并迅速使反应温度上升到170℃;
④气体通过稀NaOH溶液进行洗气后,分别通人酸性KMnO4溶液和溴水中。
据此回答下列问题:
(1)写出实验室制备乙烯的化学方程式:______。
(2)在反应液中加入少量碎瓷片的作用是_________。
(3)步骤②中温度计水银球的正确位置是___________________________________。
(4)步骤③加热时,若反应温度不能迅速升高到170℃会产生一种有机副产物,写出该物质的名称_____。
(5)将乙烯(除杂后)通人酸性KMnO4溶液中,观察到的现象是;通人溴水中发生反应的化学方程式是。
某化学创新实验小组设计了如图示实验装置来制取溴苯并证明该反应为取代反应。已知:溴苯的熔点为‒30.8℃,沸点156℃。
(1)三颈烧瓶中发生的有机反应化学方程式;
(2)仪器A的名称;本实验使用仪器A的原因。而在实验室实际实验时并没有使用A的原因是。
(3)锥形瓶中小试管内CCl4作用;如不加该部分装置将导致什么结果。
(4)分液漏斗内的NaOH溶液作用:。
为了综合利用副产品CaSO4,某化工厂与相邻的合成氨厂联合设计了下列(NH4)2SO4生产流程: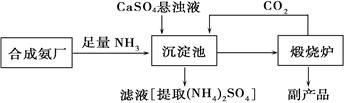
请回答以下问题:
(1)合成氨反应的化学方程式是,该反应在(填设备名)中发生,反应所用催化剂一般用。
(2)沉淀池中发生的主要反应方程式是,该反应能够发生的原因是。
(3)在上述流程中可以循环使用的物质是,该生产过程中的副产品是。
(4)从绿色化学和资源综合利用的角度说明上述流程的主要优点是。
三个化学小组的同学测定某Na2CO3固体样品(仅含NaOH杂质)的纯度,他们提出了各自的气体分析法。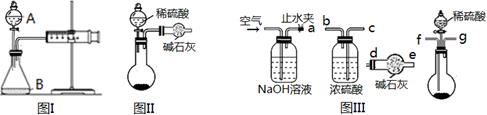
(1)第一小组用图I所示装置,仪器A的名称。把m1 g的混合物与足量稀硫酸反应后,测定产生的CO2气体的体积。实验开始时需检查该装置气密性,具体的操作方法是。
(2)第二小组用图II装置测定CO2的质量。该装置存在明显缺陷是:。
(3)第三小组在第二小组装置的基础上,解决了第二小组装置的问题。所用到的仪器如图III,装置的连接顺序是a—(填写接口字母,图中仪器可重复使用)。实验中取了样品m1 g,称量干燥管质量为m2 g,与足量稀硫酸反应后称量干燥管质量为m3 g,则Na2CO3的纯度表达式为。
(16分)某学习小组利用如图实验装置制备Cu(NH3)xSO4·H2O.并测量x值。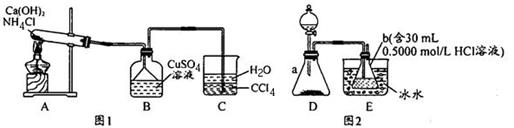
【Cu(NH3)xSO4·H2O制备】见图1
(1)A中发生的化学反应方程式为________________________________。
(2)C中CCl4的作用是 。
(3)B中先产生蓝色沉淀,随后沉淀溶解变成深蓝色溶液,此溶液中含有Cu(NH3)xSO4,若要从溶液中析出Cu(NH3)xSO4·H2O晶体,可加入试剂 。
【x值的测量】见图2
步骤一:检查装置气密性,称取0.4690 g晶体[M = (178+17x)g/mol]于锥形瓶a中
步骤二:通过分液漏斗向锥形瓶a中滴加l0%NaOH溶液至无气体产生为止
步骤三:用0.5000 mol/L的NaOH标准溶液液滴定b中剩余HCI,消耗标准溶液液16.00 mL
(4)步骤二的反应可理解为Cu(NH3)xSO4与NaOH在溶液中反应,其离子方程式为_________________。
【x值的计算与论证】
(5)计算:x = 。
该学习小组针对上述实验步骤,提出测量值(x)比理论值偏小的原因如下:
假设1:步骤一中用于称量的天平砝码腐蚀缺损;
假设2:步骤二中_____________________________________________________(任写两点);
假设3 :步骤三中测定结束读数时,体积读数偏小。该假设_______(填“成立”或“不成立”)。
(6)针对假设l,你对实验的处理意见是________________。