下列实验步骤与实验事实的相应结论解释正确的是 ( )
| 选项 |
实验步骤与实验事实 |
结论解释 |
| A |
在溶有NH3的BaCl2溶液中通入CO2,有白色沉淀生成 |
NH3是该反应的催化剂 |
| B |
钠能从熔融态的氯化钾中置换出钾 |
钠比钾活泼 |
| C |
SO2能使KMnO4溶液褪色 |
体现SO2的漂白性 |
| D |
将Cl2通入H2O2和NaOH的混合液中,产生大量气泡 |
Cl2是该反应的氧化剂 |
某学生用碱式滴定管量取0.1mol/L的NaOH溶液,开始时仰视液面读数为1.0mL, 取出部分溶液后,俯视液面,读数为11.0mL,该同学在操作中实际取出的液体体积为()
| A.大于10.0mL | B.小于10.0mL | C.等于10.0mL | D.等于11.0mL |
下列离子方程式书写不正确的是
| A.在氢氧化钡溶液中逐滴加入硫酸氢钠溶液至恰好呈中性: Ba2++2OH-+2H++SO42-====BaSO4↓+2H2O |
| B.在苯酚钠溶液中通入少量二氧化碳:C6H5O-+H2O+CO2→C6H5OH+HCO3- |
| C.在澄清石灰水中滴加过量碳酸氢钠溶液: Ca2++2HCO3-+2OH-====CaCO3↓+2H2O+ CO32- |
| D.向100mL0.2mol/L溴化亚铁的溶液中慢慢通入448mL(标准状况)Cl2: |
2Fe2++4Br-+3Cl2====2Fe3++2Br2+6Cl-
下列各组离子中,一定能大量共存的是()
| A.加入铝粉只有氢气产生的溶液中:Na+、SO42-、NO3-、Mg2+、 |
| B.滴加石蕊试液显红色的溶液中:Fe3+、NH4+、Cl-、SCN- |
| C.在0.1mol/L的NaHSO4溶液中:NH4+、Na+、Al3+、Cu2+、NO3- |
| D.在0.1mol/L的NaHCO3溶液中K+、Al3+、Fe3+、NO3- |
设NA为阿伏加德罗常数,下列有关叙述不正确的是( )
| A.常温常压下,1 mol碳烯(∶CH2)所含电子总数为8NA |
B.在标准状况下,V L水中含有的氧原子个数为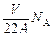 |
| C.常温时,1 L pH = 1的水溶液中水合氢离子数为0.1 NA |
| D.1 mol OH –在电解过程中被氧化,提供电子的数目为NA |
设NA为阿伏加德罗常数,则下列说法错误的是()
| A.5.6gFe 与足量的氯气反应时失去的电子数目为0.2NA |
| B.0.1molN5+离子中所含的电子数为3.4NA |
| C.1 L0.2mol/L氯化钡溶液中含氯离子的数目为0.4NA |
| D.在标准状况下,11.2LSO3所含原子数目大于2NA |