根据反应8NH3 + 3Cl2 ="=" 6NH4Cl + N2 ,回答下列问题:
(1) 还原剂是 (写化学式);
(2) 用双线桥法表示该反应电子转移的方向和数目;
(3)当反应中转移1.806×1024个电子时,被氧化的气体在标准状况下的体积为 升。
(1)9.2g氮的氧化物NOx中含有N原子数为0.2 mol,则NOx的摩尔质量为___________,x数值为_______,这些质量的NOx在标准状况的体积约为_______。
(2)V L Fe2(SO4)3溶液中含有a g SO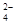 ,取此溶液0.5V L,用水稀释至2V L,则稀释后溶液中Fe3+的物质的量的浓度为_________________
,取此溶液0.5V L,用水稀释至2V L,则稀释后溶液中Fe3+的物质的量的浓度为_________________
在花瓶中加入“鲜花保鲜剂”,能延长鲜花的寿命.下表是500mL“鲜花保鲜剂”中含有的成分,阅读后回答下列问题:
| 成分 |
质量(g) |
摩尔质量(g•mol﹣1) |
| 蔗糖 |
25.00 |
342 |
| 硫酸钾 |
0.87 |
174 |
| 阿司匹林 |
0.17 |
180 |
| 高锰酸钾 |
0.316 |
158 |
| 硝酸银 |
0.02 |
170 |
(1)下列“鲜花保鲜剂”的成分中,属于非电解质的是__________.
A.蔗糖 B.硫酸钾 C.高锰酸钾 D.硝酸银
(2)配制上述“鲜花保鲜剂”所需的仪器有:烧杯、玻璃棒、药匙、____________、____________、_______________.(在横线上填写所缺仪器的名称)
(3)在溶液配制过程中,下列操作对配制结果没有影响的是__________________.
A.定容时俯视容量瓶刻度线
B.容量瓶在使用前未干燥,里面有少量蒸馏水
C.容量瓶在使用前刚刚配制完一定物质的量浓度的NaCl溶液而未洗净
D.定容摇匀后发现液面低于容量瓶的刻度线,但未做任何处理
(4)“鲜花保鲜剂”中K+(阿司匹林中不含K+)的物质的量浓度为__________mol/L.
在 2KMnO4+16HCl═2MnCl2+2KCl+5Cl2↑+8H2O反应中.
(1)______元素被氧化,氧化产物是______; 还原产物是______;氧化剂和还原剂的物质的量之比为___________.
(2)用双线桥法表示该反应的电子转移情况.
(1)写出下列反应的离子方程式:
①Ba(OH)2和CuSO4 ____________________________________.
②CuO和H2SO4 _____________________________________.
(2)写出一个能实现下列离子反应的化学方程式:
①Fe+Cu2+=Fe2++Cu _______________________________________.
②CO32﹣+2H+=CO2↑+H2O ________________________________________.
(1)标准状况下,5.6LSO2的质量为_______克,共含有________个原子.
(2)质量相同的 HCl、NH3、CO2、O2四种气体中,含有分子数目最少的是_______(填分子式,下同),在相同温度和相同压强条件下,体积最大的是______________.
(3)用托盘天平称取5.0g CuSO4•5H2O晶体,溶于水配成100mL溶液,其物质的量浓度为_____________.