现有以下物质:①NaCl晶体 ②液态SO3 ③液氯 ④铜⑤BaSO4固体⑥纯蔗糖(C12H22O11) ⑦酒精(C2H5OH) ⑧熔化的KNO3 ⑨盐酸 ⑩NH3
请回答下列问题(用序号填空):
⑴以上物质中能导电的是_________________。
⑵以上物质中属于电解质的是___________________。
⑶以上物质中属于非电解质的是____________________。
⑷以上物质中溶于水后形成的水溶液能导电的是_____________。
A~J均为有机化合物,它们之间的转化如F图所示:实验表明:①D既能发生银镜反应,又能与金属钠反应放出氢气;②I有两种不同化学环境的氢原子;③1mol J与足量金属钠反应可放出22.4L氢气(标准状况)。
请根据以上信息回答下列问题:
(1)A中官能团有(填名称),由A生成B的反应类型是______反应,
(2)D的结构简式为,由D生成E的反应类型是反应,做完此反应实验的试管可以用(填试剂名称)清洗
(3)由E生成F的化学方程式为,M是与E具有相同官能团的E的同分异构体,写出M的一种结构简式。
(4)G的结构简式为,
(5)由I生成J的化学方程式为。
I.(1)CH3OH(1)、H2的燃烧热分别为:725.5 kJ/mol和285.8 kJ/mol,写出工业上以CO2、H2合成CH3OH(1)的热化学方程式:。
(2)右图为光电解水的装置,写出光照时半导体电极表面发生的电极反应式________。目前应用最多的半导体材料是Si,甚至有人提出硅是“21世纪的能源”,硅可作为新能源的原因可能的是(填字母)。
a.在自然界中存在大量的单质硅
b.硅可以通过化学方法“再生”
c.硅具有较强的亲氧性,燃烧放出的热量多
d.硅的化学性质不活泼,便于安全贮存、运输
II.将0.2mol/L HA溶液与O.lmol/L NaOH溶液等体积混合,测得混合溶液c(Na+)>c(A—),
用“>”、“<”或“=”填写下列空白:
(1)混合溶液中c(A—)____c(HA);c(HA)+c(A—)__0.lmol/L;
(2)混合溶液中,由水电离出来的c(OH—)0.2mol/L HA溶液中由水电离出的c(H+)
(3)25℃时,如果取0.2mol/L HB溶液与0.lmol/L NaOH溶液等体积混合,测得混合溶液的pH <7,则HB的电离程度NaB的水解程度。
甲、乙为单质,丙、丁为化合物,它们之间存在如下的转化关系:
甲+丙→乙+丁
(1)若该转化关系为我国古代湿法冶炼金属乙的原理,写出此反应的离子方程式
,若该转化关系为高温火法冶炼金属乙(乙与湿法冶炼金属乙相同)的原理,且同时生成的丁是一种无色无味的有毒气体,则甲的化学式为
。
(2)若甲、乙均为非金属,丙为氧化物,则:
①乙为氧化产物时,乙可能是____(填一种物质的化学式,下同),按照元素周期表推出,此时反应物甲可能是____.
②乙为还原产物时,丁所属的物质类别是,发生的反应的化学方程式为。
一定条件下铁可以和CO2发生反应: Fe(s)+CO2(g) FeO(s)+CO(g);△H>0
FeO(s)+CO(g);△H>0
(1)一定温度下,向某密闭容器中加入足量铁粉并充入一定量的CO2气体,反应过程中CO2气体和CO气体的浓度与时间的关系如图所示,求8分钟内CO的平均反应速率v(CO)=。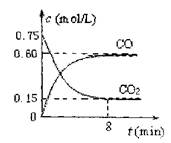
(2)下列措施中能使平衡时c(CO)/c(CO2)增大的是(填序号)。
| A.升高温度 | B.增大压强 | C.充入一定量氮气 | D.再加入一些铁粉 |
(3)反应达到平衡后,若保持容器体积不变时,再通入一定量的CO2,则CO2的转化率将(填“增大”、“减小”、“不变”)
(4)铁的重要化合物在生产生活中应用十分广泛。
①FeCl3溶液可用于天然气脱硫,写FeCl3溶液与天然气中H2S反应的离子方程式:
。
②高铁酸钠(Na2FeO4)是一种新型饮用水消毒剂。高铁酸钠生产方法之一是:强碱性溶液中用NaClO氧化Fe(OH)3生成高铁酸钠、氯化钠和另一种常见化合物,该反应的离子方程式为。
(5)已知:2CO(g)+O2(g)==2CO2(g) △H=-566 kJ/mol;2H2(g)+O2(g)==2H2O(g) △H=-483.6 kJ/mol。写出CO和H2O(g)作用生成CO2和H2的热化学方程式
。
在一定体积的密闭容器中进行如下反应:
CO2(g)+H2(g)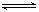 CO(g)+H2O(g);其化学平衡常数K和温度t的关系如下表:
CO(g)+H2O(g);其化学平衡常数K和温度t的关系如下表:
| t℃ |
700 |
800 |
830 |
1000 |
1200 |
| K |
0.6 |
0.9 |
1.0 |
1.7 |
2.6 |
回答下列问题:
(1)该反应的化学平衡常数表达式为K=。
(2)该反应为反应(选填“吸热”或“放热”)。
(3)能判断该反应是否达到化学平衡状态的依据是(多选扣分)。
a.容器中压强不变b.混合气体中c(CO)不变
c.υ正(H2)=υ逆(H2O)d.c(CO2)=c(CO)
(4)若向容器中投入各物质2mol,加热到800℃使进行反应,到达平衡时物质的量增加的物质是。