空气质量高低直接影响着人类的生产和生活,它越来越受到人们的关注。被污染的空气中杂质的成分有多种,其中计入《空气质量日报》空气污染指数的项目有SO2、CO、NO2、O3和可吸入颗粒物等。
请回答下列问题:
(1)S、N、O的第一电离能由大到小的顺序为 。
(2)血红蛋白中含有Fe2+,CO易与血红蛋白结合成稳定的配合物而使人中毒。
①写出亚铁离子的基态电子排布式 。
② CO有多种等电子体,其中常见的两种为 。CO结构中σ键和П键数目之比为 。
③Fe(CO)5常温下呈液态,熔点为-20.5℃,沸点为103℃,易溶于非极性溶剂,据此可判断Fe(CO)5晶体属于 ___________ (填晶体类型),Fe元素的化合价 。
(3)SO2是一种大气污染物,为减轻SO2污染,火力发电厂生产中常在燃煤中加入CaO以“固硫”。 CaO晶胞如右图所示,其中Ca2+周围的阴离子配位数为 ,CaO晶体和NaCl晶体中离子排列方式相同,其晶格能分别为:CaO:3401kJ/mol、NaCl:786kJ/mol。CaO晶体的熔点 NaCl晶体的熔点(填“高于”、“等于”或“低于”),导致两者晶格能差异的主要原因是 。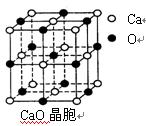
(4)随着人们生活质量的提高,不仅室外的环境安全为人们所重视,室内的环境安全和食品安全也越来越为人们所关注。甲醛是室内主要空气污染物之一(其沸点是-19.5 ℃),甲醇是“假酒”中的主要有害物质(其沸点是64.65 ℃),甲醇的沸点明显高于甲醛的主要原因是: 。
二氧化硫、一氧化碳、氮的氧化物、氨气都是非常重要的非金属化合物,研究这些化合物对环境保护、理解化学反应原理都具有重要意义。
(1)二氧化氮与一定量空气混合通入水中能被水完全吸收,反应的化学方程式为_________________。若该反应有a×NA个电子转移,则参加反应的二氧化氮的物质的量为________。
(2)下列除去大气污染物的化学方程式不正确的是________。
A.汽车尾气经催化剂作用:CO+NO NO2+C
NO2+C
B.石灰乳吸收硫酸厂尾气:SO2+Ca(OH)2===CaSO3+H2O
C.燃烧法除去尾气中硫化氢:2H2S+3O2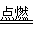 2SO2+2H2O
2SO2+2H2O
D.氨气与一氧化氮在一定条件下反应:4NH3+6NO 5N2+6H2O
5N2+6H2O
(3)大多数非金属氧化物能被氢氧化钠溶液吸收。例如,NaOH+SO2=NaHSO3,2NaOH+SO2=Na2SO3+H2O,2NO2+2NaOH=NaNO3+NaNO2+H2O,NO+NO2+2NaOH=2NaNO2+H2O,NO不溶于氢氧化钠溶液或水。
①同种反应物,其反应产物与浓度、温度、反应物相对量等因素有关。影响二氧化硫与氢氧化钠反应产物的因素与下列反应相同的是________。
A.木炭与氧气反应
B.硫与氧气反应
C.钠与氧气
D.铜与硝酸溶液反应
②某NO与NO2混合气体通入氢氧化钠溶液被完全吸收,推测混合气体中气体组成为________。
A. =1 B.
=1 B. ≤1 C.
≤1 C. ≥1 D.无法判断
≥1 D.无法判断
在已经提取氯化钠、溴、镁等化学物质的富碘卤水中,采取下面的工艺流程生产单质碘。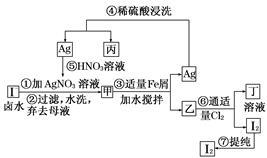
试回答下列问题:
(1)乙、丁中溶质的化学式:乙:________,丁________。
(2)第④步操作中用稀硫酸浸洗的目的是________(填写字母编号)。
| A.除去未反应的NO | B.除去未反应的I- |
| C.除去未反应的Fe | D.除去碱性物质 |
(3)第⑦步操作可供提纯I2的两种方法是________和________(不要求写具体步骤)。
(4)实验室检验I2的方法是___________________________________________________。
(5)甲物质见光易变黑,其原因是(用化学方程式表示)__________________。
过渡金属元素及其化合物的应用广泛,是科学家们进行前沿研究的方向之一。
(1)测定土壤中铁的含量时需先将三价铁还原为二价铁,再采用邻啡罗啉做显色剂,用比色法测定,若土壤中含有高氯酸盐时会对测定有干扰。相关的反应如下:
4FeCl3+2NH2OH•HCl=4FeCl2+N2O↑+6HCl+H2O
①基态Fe原子中,电子占有的最高能层符号为__________,核外未成对电子数为__________,Fe3+在基态时,外围电子排布图为______________________________。
②羟胺中(NH2OH)采用sp3杂化的原子有_______________,三种元素电负性由大到小的顺序为________;与ClO4-互为等电子体的分子的化学式为_______________________。
(2) 过渡金属原子可以与CO分子形成配合物,配合物价电子总数符合18电子规则。如Cr可以与CO形成Cr(CO)6分子:价电子总数(18)=Cr的价电子数(6)+CO提供电子数(2×6)。Fe、Ni两种原子都能与CO形成配合物,其化学式分别为_____________、______________。
(3) Pt2+的常见配合物Pt(NH3)2Cl2存在两种不同的结构:一种为淡黄色(Q),不具有抗癌作用,在水中的溶解度较小;另一种为黄绿色(P),具有抗癌作用,在水中的溶解度较大。
①Q是_________________分子(选填“极性”或“非极性”)。
②P分子的结构简式为__________________________。
(4)NiXO晶体晶胞结构为NaCl型,由于晶体缺陷,x值为0.88,晶胞边长为a pm。晶胞中两个Ni原子之间的最短距离为___________pm。若晶体中的Ni分别为Ni2+、Ni3+,此晶体中Ni2﹢与Ni3﹢的最简整数比为_________。
联合生产是实现节能减排的重要措施,工业上合成氨和硝酸的联合生产具有重要的意义。下面是工业上合成氨的简易流程: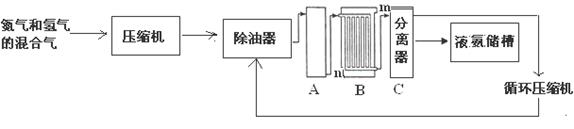
(1)设备A中含有电加热器,触媒和热交换器,设备A的名称是______________,其中发生的化学反应方程式为_________________________________________________;
(2)设备B的名称是_______________,其中m和n是两个通水口,入水口是___________(填“m”或“n”);不宜从相反方向通水的原因是__________________________________;
(3)设备C的作用是_______________________________________________。
(4)原料气中往往含有CO等杂质,在进行反应前要先净化,净化的原因是_________。
(5)氮气和氢气的混合气体通过压缩机压缩的原因是____________________________。
(6)生产出来的NH3可以用来生产硝酸。在制备硝酸的过程中,由于二氧化氮不能一次性被水完全吸收,因此生成的气体须经过多次氧化、吸收的循环操作,使其充分转化为硝酸(不考虑生产过程中的其它损失)。
①从理论上分析,要使氨气完全转化为硝酸,则原料中氧气和氨气物质的量的投料比至少为________。
②如果按理论上的原料比将原料放在特定条件的密闭容器中进行反应,所有物质不与外界交换,则最后所得溶液的质量分数为____________________。(保留三位有效数字)
汽车在现代生活中扮演着越来越重要的角色,但其尾气(碳氢化合物、氮氧化物及一氧化碳等)带来的环境污染越来越明显,汽车尾气的治理已经迫在眉睫。
(1)尾气中的CO主要来自于汽油的不完全燃烧。
①有人设想按下列反应除去CO:2CO(g)=2C(s)+O2(g)ΔH= +221kJ·mol-1,简述该设想能否实现______(填“是”或“否”)依据是:_______________________________________。
②研究表明:反应CO(g)+H2O(g) H2(g)+CO2(g)平衡常数随温度的变化如下表所示:
H2(g)+CO2(g)平衡常数随温度的变化如下表所示:
| 温度/℃ |
400 |
500 |
800 |
| 平衡常数K |
9.94 |
9 |
1 |
该反应的ΔH______0(填“>”或“<”)若反应在500℃时进行,设起始时CO和H2O的浓度均为0.020mol·L﹣1,在该条件下达到平衡时,CO的转化率为 。
(2)用CO做燃料电池电解NaCl溶液、FeCl3和FeCl2混合液的示意图如图1所示,其中A、B、D均为石墨电极,C为铜电极,转移0.4mol e-后,断开K。
①乙中产生的气体在标准状况下的体积为 。
②丙装置溶液中金属阳离子的物质的量与转移电子的物质的量变化关系如图2所示,反应结束后,要使丙装置中金属阳离子恰好完全沉淀,需要 mL 5.0mol·L﹣1 NaOH溶液。
(3)电解法处理氮氧化合物是目前大气污染治理的一个新思路,原理是将NOx在电解池中分解成无污染的N2和O2除去,如图示,两电极间是固体氧化物电解质,在一定条件下可自由传导O2-,电解池阴极反应为__________________。
(4)尾气中的碳氢化合物,如甲烷,可以用来制备氢气。其反应方程式为:
CH4(g)+H2O(g) CO(g)+3H2(g)ΔH = +206.2kJ/mol [其中投料比n(CH4):n(H2O)=1:1]。对于气相反应,用某组分(B)的平衡压强(PB)代替物质的量浓度(cB)也可表示平衡常数(记作KP,分压=总压×物质的量分数)。平衡时CH4的转化率与温度、压强(总压)的关系如图所示:
CO(g)+3H2(g)ΔH = +206.2kJ/mol [其中投料比n(CH4):n(H2O)=1:1]。对于气相反应,用某组分(B)的平衡压强(PB)代替物质的量浓度(cB)也可表示平衡常数(记作KP,分压=总压×物质的量分数)。平衡时CH4的转化率与温度、压强(总压)的关系如图所示:
则p1__ p2 (填“>”或“<”),p2时M点的平衡常数KP=________(小数点后保留3位)。