在实验室里可用右图所示装置制取氯酸钾、次氯酸钠和探究氯水的性质。
图中:①为氯气发生装置;②的试管里盛有15 mL 30% KOH溶液,并置于水浴中;③的试管里盛有15 mL 8% NaOH溶液,并置于冰水浴中;④的试管里加有紫色石蕊试液;⑤为尾气吸收装置。请填写下列空白: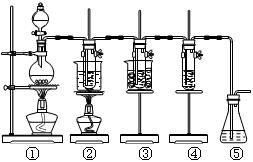
(1)装置①是氯气发生装置,蒸馏烧瓶中盛放MnO2固体,其反应的化学方程式为 ▲ 。
(2)如果实验室中MnO2用完了,则下列物质可能可以用来代替MnO2制Cl2的是: ▲ 。
| A.NaBiO3 | B.FeCl3 | C.PbO2 | D.Na2O2 |
已知氧化性强弱顺序为:NaBiO3>PbO2>MnO2>Na2O2>FeCl3 (3)比较制取氯酸钾和次氯酸钠的条件,二者的差异是
(3)比较制取氯酸钾和次氯酸钠的条件,二者的差异是
① ▲ ; ② ▲ 。
(4)反应完毕经冷却后,②的试管中有大量晶体析出。右图中符合该晶体溶解度曲线的是 ▲ (填写编号字母);从②的试管中分离出该晶体的方法是 ▲ (填写实验操作名称)。
(5)根据④的试管里紫色石蕊试液的颜色变化可否证明氯气的强氧化性 ▲ 。
为什么? ▲ 。
(6)若②的试管溶液中不但有KClO3生成还有KClO生成,且二者的物质的量之比为1∶2,则该反应中氧化剂和还原剂的物质的量之比为: ▲ 。
已知下列数据:Fe(s) + 1/2O2(g) = FeO(s) ΔH=-272kJ/mol;2Al(s) + 3/2O2(g) = Al2O3(s) ΔH=-1675kJ/mol;则2Al(s) + 3FeO(s) = Al2O3(s) + 3Fe(s)的ΔH是
| A.-859 kJ/mol | B.+859 kJ/mol | C.-1403 kJ/mol | D.-2491 kJ/mol |
下列有关吸热反应、放热反应的叙述中,正确的是
①如果反应物的总能量低于生成物的总能量,该反应一定是吸热反应。
②只要是在加热条件下进行的反应,一定是吸热反应
③只要是在常温常压下进行的反应,一定是放热反应
④中和反应和燃烧反应都是放热反应
⑤化合反应都是放热反应
⑥原电池反应可能是放热反应,也可能是吸热反应
| A.① ④ | B.① ② ③ | C.④ ⑤ ⑥ | D.① ④ ⑤ ⑥ |
有Al、CuO、Fe2O3组成的混合物共10.0 g,放入500 mL某浓度的盐酸溶液中,混合物完全溶解,当再加入250 mL 2.0 mol/L的NaOH溶液时,得到的沉淀最多。上述盐酸溶液的浓度为
| A.0.5 mol/L | B.1.0 mol/L |
| C.2.0 mol/L | D.3.0 mol/L |
甲、乙、丙、X是中学化学中常见的4种物质,其转化关系符合图。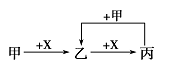
其中甲和X不可能是
| A.甲为Fe,X为Cl2 |
| B.甲为SO2,X为NaOH溶液 |
| C.甲为C,X为O2 |
| D.甲为AlCl3溶液,X为NaOH溶液 |
下列离子方程式书写正确的是
| A.Na2O2溶于水产生O2:Na2O2+H2O=2Na++2OH-+O2↑ |
B.向 NaHSO4溶液中滴加Ba(OH)2溶液至中性: H++SO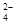 +Ba2++OH- +Ba2++OH-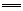 BaSO4↓+H2O BaSO4↓+H2O |
| C.用氯化铁溶液腐蚀铜板:Cu+Fe3+===Cu2++Fe2+ |
| D.用烧碱溶液吸收氯气:Cl2+2OH-==Cl-+ClO-+H2O |