根据要求完成下列各小题实验目的。(a、b为弹簧夹,加热及固定装置已略去)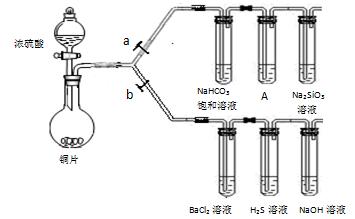
(1)验证碳、硅非金属性的相对强弱。(已知酸性:亚硫酸>碳酸)
①连接仪器、 、加药品后,打开a关闭b ,然后滴入浓硫酸,加热。
,然后滴入浓硫酸,加热。
②铜与浓硫酸反应的化学方程式是 。装置A中试剂是 。
③能说明碳的非金属性比硅强的实验现象是 。
(2)验证SO2的氧化性、还原性和酸性氧化物的通性。
①在(1)①操作后打开b,关闭a。
② H2S溶液中有浅黄色浑浊出现,化学方程式是 。
③ BaCl2溶液中无明显现象,将其分成两份,分别滴加下列溶液,将产生的沉淀的化学式填入下表相应位置。
| 滴加的溶液 |
氯水 |
氨水 |
| 沉淀的化学式 |
|
|
写出其中SO2显示还原性生成沉淀的离子方程式 。
(10分)成都七中文艺青年小组进行了关于“活泼金属与酸反应”的实验,得出了一些有趣的想法,请你帮助他们,完成一些判断。将5.4g铝片投入500mL 0.5 mol·L-1的硫酸溶液中,下图为反应产氢速率与反应时间的关系图。
(1)关于图像的描述不正确的是_③_____(2分)
①a→c段产生氢气的速率增加较快可能是表面的氧化膜逐渐溶解,加快了反应的速率
②a→c段产生氢气的速率增加较快可能是该反应放热,导致温度升高,加快了反应
③c以后,产生氢气的速率逐渐下降可能是铝片趋于消耗完全
(2)书写O→a段所对应的离子方程式____________________________________(2分)
(3)若其他条件不变,现换用500mL1mol·L-1盐酸,产生氢气速率普遍较使用500mL 0.5mol·L-1硫酸的快,可能的原因是_②④_______(2分)
①盐酸中c(H+)的浓度更大②Cl—有催化作用③SO42—有催化作用
④SO42—有阻化作用⑤Al3+有催化作用
(4)根据所学,若要加快铝片与硫酸溶液制H2的反应速率,小组成员提出一系列方案,比如:①加入某种催化剂;②滴加少量CuSO4溶液;③将铝片剪成100条;④增加硫酸的浓度至18mol/L;⑤加入蒸馏水;⑥加入少量KNO3溶液;⑦_____________。(2分)
其中,你认为不合理的方案有_____________(2分),并请你再补充一种合理方案,填入空白⑦处。
为了研究外界条件对H2O2分解速率的影响,某同学做了以下实验,请回答下列问题。
| 编号 |
操作 |
实验现象 |
| ① |
分别在试管A、B中加入5mL 5%H2O2溶液,各滴入2滴1 mol/L FeCl3溶液。待试管中均有适量气泡出现时,将试管A放入盛有5℃左右冷水的烧杯中;将试管B放入盛有40℃左右热水的烧杯中。 |
试管A中产生气泡量减少;试管B中产生的气泡量增大。 |
| ② |
另取两支试管分别加入5mL 5%H2O2溶液和5mL 10%H2O2溶液 |
试管A、B中均未明显见到有气泡产生。 |
(1)过氧化氢分解的化学方程式为________。
(2)实验①的目的是________。
(3)实验②未观察到预期的实验现象,为了帮助该同学达到实验目的,你提出的对上述操作的改进意见是_______(用实验中所提供的几种试剂)。
(4)某同学在50 mL一定浓度的H2O2溶液中加入一定量的二氧化锰,放出气体的体积(标准状况下)与反应时间的关系如下图所示,则A、B、C三点所表示的瞬时反应速率最快的是______(填“A”或“B”或“C”)。
(5)对于H2O2分解反应,Cu2+也有一定的催化作用。为比较Fe3+和Cu2+对H2O2分解的催化效果,某化学研究小组的同学分别设计了如图甲、乙所示的实验。请回答相关问题: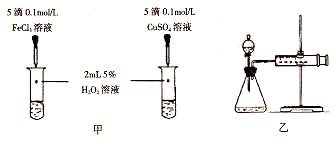
①定性分析:如图甲可通过观察_________,定性比较得出结论。有同学提出将FeCl3改为Fe2(SO4)3更为合理,其理由是_______。
②定量分析:用图乙所示装置做对照实验,实验时均以生成40 mL气体为准,其他可能影响实验的因素均已忽略。实验中需要测量的数据是_________。
14分)某学生为了探究锌与盐酸反应过程中的速率变化,他在100mL稀盐酸中加入足量的锌粉,用带刻度的集气瓶排水法收集氢气,每隔1分钟记录一次数据(累计值):
| 时间(min) |
1 |
2 |
3 |
4 |
5 |
| 氢气体积(mL) |
50 |
120 |
232 |
290 |
310 |
(1)从0~3分钟时间段内,产生氢气的速率是如何变化的?答:___________________。
造成这种变化的主要因素是_________________;从3~5分钟时间段内,产生氢气的速率是如何变化的?答:_________。造成这种变化的主要因素是_____________________。
(2)在盐酸中分别加入等体积的下列溶液,能减缓反应速率而又不减少产生氢气的量的是___________(双选题,漏选得1分,多选,错选得0分)。
A.蒸馏水 B.NaCl溶液 C.Na2CO3溶液 D.CuSO4溶液
(3)在0~1、1~2、2~3、3~4、4~5分钟五个时间段中,反应速率最大的是在____分钟时间段内,在该时间段内盐酸的反应速率为(设溶液体积不变,上述气体体积为标况下数据)。
.某学生根据石蜡油在碎瓷片或氧化铝催化作用下能分解得到乙烯的性质,设计下图的实验装置。据图回答: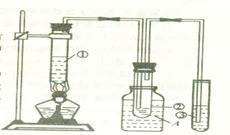
(1)试管①中盛的是_____________________;
(2)试管①至试管②上部导管的作用是______;
(3)装置A的作用是_______________________;
(4)试管③中盛的是__________________,反应后观察到的现象是___________________;
(5)若往试管②的液体中滴入溴的四氯化碳溶液,发现溴的颜色褪去,则说明液体中含有___________烃。
以下是某课题组设计的由烃A合成聚酯类高分子材料。 的路线:
的路线: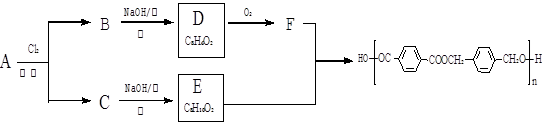
已知同一碳原子上连两个羟基时结构不稳定,易脱水生成醛或酮。
根据以上信息回答:
(1)A的分子式,F中官能团的名称是。
(2)化合物D的结构简式是,由B生成D的反应过程中生成的不稳定中间体的结构简式是,该中间体生成D的反应类型为。
(3)E与F反应的化学方程式是,反应类为。与E具有相同官能团的含苯环的同分异构体有(写结构式)。