下列检验离子的方法及结论正确的是( )。
| A.向某溶液中滴加AgNO3溶液后产生白色沉淀,说明原溶液中含有Cl- |
| B.向某溶液中滴加BaCl2溶液后产生白色沉淀,说明原溶液中含有SO42- |
| C.向某溶液中滴加NaOH溶液后生成蓝色沉淀,说明原溶液中含有Cu2+ |
| D.向某溶液中滴加稀硫酸后生成无色无味的气体,说明原溶液中含有CO32- |
在一密闭容器中,反应aA(g) bB(g)达平衡后,保持温度不变,将容器体积增加一倍,当达到新的平衡时,A的浓度变为原来的60%,则
bB(g)达平衡后,保持温度不变,将容器体积增加一倍,当达到新的平衡时,A的浓度变为原来的60%,则
| A.平衡向正反应方向移动了 | B.平衡向逆反应方向移动了 |
| C.物质B的质量分数增加了 | D.a<b |
下列变化过程中,ΔS<0的是
A.氯化钠溶于水中 B.NH3(g)和HCl(g)反应生成NH4Cl
C .干冰的升华 D.CaCO3(S)分解为CaO(S)和CO2(g)
.干冰的升华 D.CaCO3(S)分解为CaO(S)和CO2(g)
在2A+B 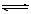 3C+4D反应中,表示该反应速率最快
3C+4D反应中,表示该反应速率最快 的是
的是
A.v(A)=0.5 mol·L-1·s-1 B.v(B)=0.3 mol·L-1·s-1
C.v(C)=0.8 mol·L-1·s-1 D.v(D)=1 mol·L-1·s-1
amol FeO与bmol Cu2S投入到Cmol/L的硝酸中恰好完全反应,生成NO共消耗硝酸VL,所得澄清溶液成分可看作为Fe(NO3)3、Cu(NO3)2、H2SO4的混合液,则反应中未被还原的硝酸不可能为()
| A.(189a+252b)g | B. |
C.(3a +2b)×63g +2b)×63g |
D.(3a+4b)mol |
肼(N2H4)一空气燃料电池是一种环保型碱性燃料电池,其电解质是20%—30%的KOH溶液。电池总反应为:N2H4+O2=N2↑+2H2O。下列关于该燃料电池工作时的说法正确的是()
| A.溶液中阴离子的浓度基本不变 |
| B.正极的电极反应式:N2H4+4OH--4e-=4H2O+N2↑ |
| C.正极的电极反应式是:O2+4H++4e-=2H2O |
| D.溶液中的阴离子向负极移动 |