下图是中学化学中常用于混合物的分离和提纯的装置,请根据装置回答问题:
(1)从氯化钠溶液中得到氯化钠固体,选择装置 (填代表装置图的字母,下同);除去自来水中的Cl-等杂质,选择装置 ;从碘水中分离出I2,选择装置 ,该分离方法的名称为 。
(2)装置A中①的名称是 ,进冷却水的方向是 。
装置B在分液时为使液体顺利下滴,应进行的具体操作是 
 。(3)实验室中制取的Fe(OH)3胶体中常常含有杂质Cl-离子。可用 的方法除去
。(3)实验室中制取的Fe(OH)3胶体中常常含有杂质Cl-离子。可用 的方法除去
Fe(OH)3胶体中混有的杂质Cl-离子。
(NH4)2Fe(SO4)2·6H2O俗名摩尔盐,价格便宜,可用来净水或治疗缺铁性贫血等,是一种重要的化工原料。
(1)摩尔盐的水溶液呈色。
(2)c(Fe2+)相同的摩尔盐和硫酸亚铁两溶液比较,物质的量浓度较大的是。
(3)甲乙两位同学想测定一瓶摩尔盐的纯度。甲同学设计的实验装置如下图: 。
。
从上图推断甲同学想通过测定计算摩尔盐的纯度。该方案的不足之处在于。
(4)乙同学在甲同学的基础上做了改进,其实验装置如下图: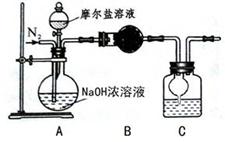 。
。
则B与C中的试剂分别是和。C中干燥管的作用是。乙同学称取了 10.0g的摩尔盐样品,若实验完毕后测得洗气瓶及瓶内溶液共增重 0.68g,则依此数据推算这份摩尔盐的纯度为%(答案精确到小数点后第一位)。
硝酸是一种重要的工业原料,工业制硝酸的关键是氨的催化氧化,与硝酸工业相关的过程中产生的氮氧化物的处理与应用也是科学研究的热点。
图10、图11分别是实验室模拟合成氨及氨催化氧化的装置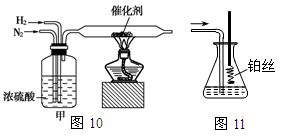
(1)氮气和氢气通过图10装置,该装置中浓硫酸的作用是控制气体流速和。
(2)用图11装置吸收一段时间氨后,再通入空气,同时将已经加热的铂丝插入乙装置的锥形瓶内,铂丝保持红热的原因是,写出该装置中氨氧化的化学方程式。反应结束后锥形瓶内的溶液中含有H+、OH-、离子、离子。
钠是活泼的碱金属元素,钠及其化合物在生产和生活中有广泛的应用。
完成下列计算:
(1)叠氮化钠(NaN3)受撞击分解产生钠和氮气,故可应用于汽车安全气囊。若78克叠氮化钠完全分解,产生标准状况下氮气___________________L 。
(2)钠-钾合金可在核反应堆中用作热交换液。5.05 g钠-钾合金溶于200 mL水生成0.075 mol氢气。计算溶液中氢氧化钠的物质的量浓度______________________(忽略液体体积变化)。
(3)氢氧化钠溶液处理铝土矿并过滤,得到含铝酸钠的溶液。向该溶液中通入二氧化碳,有下列反应: 2NaAl(OH)4+CO2→2Al(OH)3↓+Na2CO3+H2O。己知通入二氧化碳112 L(标准状况下),生成的Al(OH)3和Na2CO3的物质的量之比为4:5。若向该溶液中通入的二氧化碳为224L(标准状况下),计算生成的 Al(OH)3和Na2CO3的物质的量的最大值。
某学生利用以下装置探究氯气与氨气之间的反应。其中A、F分别为氨气和氯气的发生装置,C为纯净干燥的氯气与氨气反应的装置。
请回答下列问题:
(1)装置F中发生反应的离子方程式:______________________________________。
(2)装置A中的烧瓶内固体可选用_________(选填以下选项的代号)。
A.碱石灰B.生石灰 C.二氧化硅D.五氧化二磷
(3)虚线框内应添加必要的除杂装置,请从上图的备选装置中选择,并将编号填入下列空格:B,D_____________,E。(均填编号)
(4)催化剂存在下,NH3可用来消除NO的污染,生成两种对环境无害的物质。写出该反应的化学方程式:;该反应中每生成0.5molN2转移mol电子。
(14分)利用废铝箔(主要成分为Al、少量的Fe、Si等)既可制取有机合成催化剂AlBr3又可制取净水剂硫酸铝晶体[A12(SO4)3•18H2O]。
I.实验室制取无色的无水AlBr3(熔点:97.5℃,沸点:263.3~265℃)可用如图所示装置
主要实验步骤如下:
步骤l:将铝箔剪碎,用CCl4浸泡片刻,干燥,然后投入到烧瓶6中。
步骤2:从导管口7导入氮气,同时打开导管口l和4放空,一段时间后关闭导管口7和1;导管口4接装有P2O5的干燥管。
步骤3:从滴液漏斗滴入一定量的液溴于烧瓶6中,并保证烧瓶6中铝过剩。
步骤4:加热烧瓶6,回流一定时间。
步骤5:将氮气的流动方向改为从导管口4到导管口l。将装有P2O5的干燥管与导管口1连接,将烧瓶6加热至270℃左右,使溴化铝蒸馏进入收集器2。
步骤6:蒸馏完毕时,在继续通入氮气的情况下,将收集器2从3处拆下,并立即封闭3处。
(1)步骤l中,铝箔用CCl4浸泡的目的是。
(2)步骤2操作中,通氮气的目的是。
(3)步骤3中,该实验要保证烧瓶中铝箔过剩,其目的是。
(4)步骤4依据何种现象判断可以停止回流操作。
(5)步骤5需打开导管口l和4,并从4通入N2的目的是。
II.某课外小组的同学拟用废铝箔制取硫酸铝晶体,已知铝的物种类别与溶液pH关系如图所示。
实验中可选用的试剂:①处理过的铝箔;②2.0 mol•L-1硫酸;③2.0mol•L-1NaOH溶液。
(6)由铝箔制备硫酸铝晶体的实验步骤依次为:
①称取一定质量的铝箔于烧杯中,分次加入2.0 mol•L-1NaOH溶液,加热至不再产生气泡为止。
②过滤。
③。
④过滤、洗涤。
⑤。
⑥蒸发浓缩。
⑦冷却结晶。
⑧过滤、洗涤、干燥。