下列叙述正确的是( )
| A.摩尔是国际科学界建议采用的一种物理量 |
| B.物质的摩尔质量等于该物质的相对分子质量 |
| C.O22-离子的摩尔质量是32 g·mol-1 |
| D.1 mol H2O的质量为18 g·mol- |
.对于可逆反应C(s)+H2O(g) CO(g)+H2(g) ,ΔH>0,达到平衡,下列说法正确的是( )
CO(g)+H2(g) ,ΔH>0,达到平衡,下列说法正确的是( )
| A.升高温度,平衡向逆反应方向移动 |
| B.加入固体碳,平衡向正反应方向移动 |
| C.加入水蒸气,平衡向逆反应方向移动 |
| D.扩大容器体积,平衡向正反应方向移动 |
可逆反应mA(固)+nB(气) eC(气)+fD(气),反应过程中,当其它条件不变时,C的百分含量(C%)与温度(T)和压强(P)的关系如下图:下列叙述正确的是
eC(气)+fD(气),反应过程中,当其它条件不变时,C的百分含量(C%)与温度(T)和压强(P)的关系如下图:下列叙述正确的是 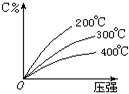
| A.达平衡后,加入催化剂则C%增大 |
| B.达平衡后,若升温,平衡左移 |
| C.化学方程式中n<e+f |
| D.达平衡后,增加A的量有利于平衡向右移动 |
.下列叙述中,能用勒夏特列原理解释的是
| A.向反应体系中加入催化剂以加快化学反应速率 |
| B.温度越高,化学反应速率越快 |
| C.由H2(g)、I2(g)、HI(g)组成的平衡体系加压后颜色变深 |
| D.温度越高, 工业合成氨的产率越低 |
把下列四种x溶液,分别加入四个盛有10mL 2mol·L-1盐酸的烧杯中,均加水稀释到50mL,此时x和盐酸缓慢进行反应。其中反应速率最大的是
| A.20ml 3mol·L-1的x溶液 | B.20ml 2mol·L-1的x溶液 |
| C.10ml 4mol·L-1的x溶液 | D.10mL 2mol·L-1的x溶液 |
有一处于平衡状态的反应X(s)+3Y(g) 2Z(g)(
2Z(g)(
△H<0)。为了使平衡向生成Z的方向移动,应选择的条件是
①升高温度 ②降低温度 ③增大压强
④降低压强 ⑤加入正催化剂 ⑥分离出Z
| A.①③⑤ | B.②③⑤ | C.②③⑥ | D.②④⑥ |