用50mL0.50mol/L盐酸与50mL0.55mol/LNaOH溶液在如图所示的装置中进行中和反应。通过测定反应过程中所放出的热量可计算中和热。
回答下列问题:
(1)从实验装置上看,图中尚缺少的一种玻璃用品是 。
(2)烧杯间填满碎纸条的作用是 。
(3)大烧杯上如不盖硬纸板,求得的中和热数值 (填“偏大、偏小、无影响”)
(4) 如果用60
如果用60 mL0.50mol/L盐酸与50mL0.55mol/LNaOH溶液进行反应,与上述实验相比,所放出的热量 (填“相等、不相等”),所求中和热 (填“相等、不相等”),
mL0.50mol/L盐酸与50mL0.55mol/LNaOH溶液进行反应,与上述实验相比,所放出的热量 (填“相等、不相等”),所求中和热 (填“相等、不相等”),
对于实验Ⅰ~Ⅳ的实验现象预测正确的是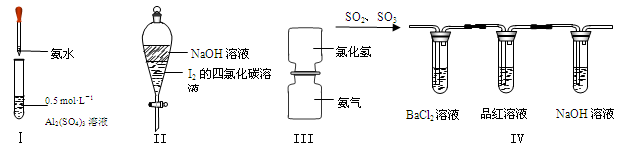
| A.实验I:试管中先出现白色胶状物质,后溶解 |
| B.实验II:振荡后静置,下层溶液颜色保持不变 |
| C.实验III:抽去中间玻璃片,瓶内产生白烟 |
| D.实验IV:BaCl2溶液变浑浊,品红溶液褪色 |
短周期元素甲、乙、丙、丁的原子序数依次增大,甲位于第VA族,乙原子的核外电子数比甲原子多1,乙与丁同族,丙原子最外层电子数与电子层数相等,则
| A.原子半径:丙>丁>乙 |
| B.甲的气态氢化物的水溶液呈酸性 |
| C.丙与乙形成的化合物具有两性 |
| D.同周期元素中丁的最高价氧化物对应的水化物的酸性最强 |
某小组为研究电化学原理,设计如图装置,下列叙述正确的是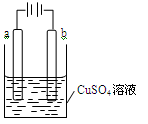
| A.若a和b为石墨,通电后a电极上发生的反应为Cu2++2e-=Cu |
| B.若a和b为石墨,通电后滴入酚酞,a电极附近溶液呈红色 |
| C.若a为铜,b为铁,通电后Cu2+向a电极移动 |
| D.若a为粗铜,b为纯铜,通电后b电极质量增加 |
对于0.1 mol·L-1 NH4Cl溶液,正确的是
| A.升高温度,溶液pH升高 |
| B.通入少量HCl气体,c(NH4+)和c(Cl-)均增大 |
| C.c(NH4+)+ c(OH-)=c(Cl-)+ c(H+) |
| D.c(Cl-)> c(H+)> c(NH4+)> c(OH-) |
某同学用滤纸折成一个纸蝴蝶并喷洒一种溶液(保持湿润),挂在铁架台上。另取一只盛某种溶液的烧杯,放在纸蝴蝶的下方(如图)。过一会,发现纸蝴蝶变为蓝色。下表的组合中,能够实现上述变化的是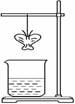
| A |
B |
C |
D |
|
| 纸蝴蝶上的喷洒液 |
酚酞 |
KI-淀粉溶液 |
石蕊 |
品红 |
| 小烧杯中的溶液 |
浓氨水 |
浓氯水 |
浓盐酸 |
浓硫酸 |