某研究性学习小组研究HNO3的氧化性,设计了如下实验:在盛有新配制的FeSO4溶液的试管中滴入2滴KSCN溶液,观察现象,然后再加入浓HNO3,溶液的颜色变红,但是将红色溶液放置一会儿则发现溶液由红色快速变为蓝色,并产生红棕色气体,这一奇特现象激起了同学们的好奇心与求知欲望,他们对此现象设计了探究性实验。
(1)甲同学认为是溶液中的Fe2+的干扰造成的,大家经过理性分析,认为可以排除Fe2+的干扰,理由是 。
(2)乙同学认为红色消失,说明Fe(SCN)3被破坏,红棕色NO2说明了某些离子与HNO3发生了氧化还原反应,推测可能是KSCN与HNO3作用。根据C、S、N的原子结构和共价键的相关知识推断SCN-的结构式为 。
(3)根据乙同学的,观点,设计了实验方案1,往浓HNO3中逐滴加入KSCN溶液,实验开始时无明显现象,一段时间后溶液慢慢变红色至深红色 ,突然剧烈反应产生大量气泡,放出红棕色气体,而溶液红色消失变为浅绿色,溶液温度升高;继续滴入KSCN溶液变为浅蓝色,最后变为无色。将产生的气体通入过量的Ba(OH)2溶液,产生浑浊,并剩余一种非极性气体;向反应后的溶液中加入BaCl2溶液产生白色沉淀。(此过程中溶液颜色变化不必细究),请写出向浓HNO3中滴入KSCN离子的方程式: 。
,突然剧烈反应产生大量气泡,放出红棕色气体,而溶液红色消失变为浅绿色,溶液温度升高;继续滴入KSCN溶液变为浅蓝色,最后变为无色。将产生的气体通入过量的Ba(OH)2溶液,产生浑浊,并剩余一种非极性气体;向反应后的溶液中加入BaCl2溶液产生白色沉淀。(此过程中溶液颜色变化不必细究),请写出向浓HNO3中滴入KSCN离子的方程式: 。
(4)丙同学认为SCN-的性质 还可进一步探究,设计了方案2,向Fe(SCN)3中分别滴加过量的氯水.溴水,溶液的红色均消失变为黄色,而加入过量的碘水时溶液的颜色基本不变。丙同学的设计意图是 。
(5)通过本次探究,可知用SCN-间接检验Fe2+时应注意 。
(12分)从铝土矿(主要成分是Al2O3,含SiO2、Fe2O3、MgO等杂质)中提取氧化铝的两种工艺流程如下:
请回答下列问题:
⑴流程甲中,固体A的主要成分是______(填化学式,下同),沉淀B的主要成分是_______,生成沉淀C的离子方程式为__________________。
⑵流程乙中,加过量烧碱时发生反应的离子方程式为________________,沉淀E的主要成分是_________。
⑶生成沉淀F的离子方程式为____________________________________。
(12)氨是重要的无机化工原料,也是合成氮肥的主要原料,因此合成氨在国民经济中占有重要地位。
⑴工业合成氨反应的化学方程式为。
⑵恒温下,向一个2L的密闭容器中充入1mol N2和2.6mol H2,20min时,反应达到平衡,容器内c(NH3)为0.08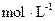 ,则c(H2)=,20min内,用N2浓度的变化表示的反应速率为。
,则c(H2)=,20min内,用N2浓度的变化表示的反应速率为。
⑶某温度下,向一个2L的密闭容器中充入1mol N2和3mol H2,在恒温下反应,以下能说明反应达到平衡状态的是
①单位时间内消耗0.1molN2的同时生成0.2molNH3
②单位时间内生成0.3molH2的同时生成0.2molNH3
③n(N2)∶n(H2 )∶n(NH3)=1∶3∶2
)∶n(NH3)=1∶3∶2
④c(NH3)=0.08mol/L
⑤容器内压强不变
⑷工业上约有80%的氨用于制造化肥。某化肥厂生产铵态氮肥(NH4)2SO4的反应可表示为:Ca SO4+2NH3+CO2+H2O= CaCO3+(NH4)2SO4
SO4+2NH3+CO2+H2O= CaCO3+(NH4)2SO4
①反应前先将CaSO4磨成粉末,加入水中制成悬浊液,则所得分散系中分散质粒子直径10-7m(填“>”或“<”)。
②向CaSO4悬浊液中通入气体时,需先通入足量NH3再通入CO2,原因是。
(12分)短周期元素Q、R、T、W在元素周期表中的位置如图所示,其中Q所处的周期序数是其主族序数的一半,请回答下列问题:
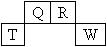
 ⑴T的原子结构示意图为_____________。
⑴T的原子结构示意图为_____________。 ⑵原子的得电子能力:Q______W(填“强于”或“弱于”)。
⑵原子的得电子能力:Q______W(填“强于”或“弱于”)。 ⑶原子序数比R多1的元素的一种氢化物能分解为它的另一种氢化物,此分解反应的化学方程式是________________________________。
⑶原子序数比R多1的元素的一种氢化物能分解为它的另一种氢化物,此分解反应的化学方程式是________________________________。 ⑷W的单质与其最高价氧化物对应的水化物的浓溶液共热能发生反应,生成
⑷W的单质与其最高价氧化物对应的水化物的浓溶液共热能发生反应,生成 两种物质,其中一种是气体,
两种物质,其中一种是气体, 反应的化学方程式为_______________。
反应的化学方程式为_______________。 ⑸R有多种氧化物,其中甲的相对分子质量最小。在一定条件下,2L的甲气体与0.5L的氧气相混合,若该混合气体被足量的NaOH溶液完全吸收后没有气体残留,所生成的R的含氧酸盐的化学式是___________。
⑸R有多种氧化物,其中甲的相对分子质量最小。在一定条件下,2L的甲气体与0.5L的氧气相混合,若该混合气体被足量的NaOH溶液完全吸收后没有气体残留,所生成的R的含氧酸盐的化学式是___________。
2010年美、日三位科学家因钯(Pd)催化的交叉偶联反应获诺贝尔化学奖。一种钯催化的交叉偶联反应如下:
( 、
、 为烃基或其他基团)
为烃基或其他基团)
应用上述反应原理合成防晒霜主要成分K的路线如下图所示(部分反应试剂和条件未注明):
已知:①B能发生银镜反应,1 mol B最多与2 mol H2反应。
②C8H17OH分子中只有一个支链,且为乙基,其连续氧化的产物能与NaHCO3反应生成CO2,其消去产物的分子中只有一个碳原子上没有氢。
③G不能与NaOH溶液反应。
④核磁共振图谱显示J分子有3种不同的氢原子。
请回答:
(1)B中含有的官能团的名称____________。
(2)B→D的反应类型___________。
(3)D→E的化学方程式___________。
(4)有机物的结构简式:G___________;K___________。
(5)符合下列条件的同分异构体有(包括顺反异构)__________种:其中一种的结构简式是___________。
a. 与D互为同系物 b. 相对分子质量是86
(6)分离提纯中间产物E的操作:先用碱除去D和H2SO4,再用水洗涤,弃去水层,最终通过___________操作除去C8H17OH,精制得E。
迷迭香酸是存在于许多植物中的一种多酚,具有抗氧化、延缓衰老、减肥降脂等功效,其结构如下图所示。
某同学设计了迷迭香酸的合成线路:
已知:①
 、
、 表示烃基或氢原子;
表示烃基或氢原子;
②苯环上的羟基很难直接与羧酸发生酯化反应。
(1)迷迭香酸分子中所含官能团的名称是羟基、碳碳双键、___________和___________。
(2)A的结构简式为___________。
(3)C的结构简式为___________。
(4)D、E反应的化学方程式为______________________。
(5)与E互为同分异构体且同时满足下列条件的有机物有____种,写出其中任意两种同分异构体的结构简式:___________、__________。
①苯环上共有四个取代基,且苯环上只有一种化学环境的氢原子;
②1mol该同分异构体分别与NaHCO3、NaOH反应时,最多消耗NaHCO3、NaOH的物质的量分别是1mol、4mol。