(12)氨是重要的无机化工原料,也是合成氮肥的主要原料,因此合成氨在国民经济中占有重要地位。
⑴工业合成氨反应的化学方程式为 。
⑵恒温下,向一个2L的密闭容器中充入1mol N2和2.6mol H2,20min时,反应达到平衡,容器内c(NH3)为0.08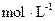 ,则c(H2)= ,20min内,用N2浓度的变化表示的反应速率为 。
,则c(H2)= ,20min内,用N2浓度的变化表示的反应速率为 。
⑶某温度下,向一个2L的密闭容器中充入1mol N2和3mol H2,在恒温下反应,以下能说明反应达到平衡状态的是
①单位时间内消耗0.1molN2的同时生成0.2molNH3
②单位时间内生成0.3molH2的同时生成0.2molNH3
③n(N2)∶n(H2 )∶n(NH3)=1∶3∶2
)∶n(NH3)=1∶3∶2
④c(NH3)=0.08mol/L
⑤容器内压强不变
⑷工业上约有80%的氨用于制造化肥。某化肥厂生产铵态氮肥(NH4)2SO4的反应可表示为:Ca SO4+2NH3+CO2+H2O= CaCO3+(NH4)2SO4
SO4+2NH3+CO2+H2O= CaCO3+(NH4)2SO4
①反应前先将CaSO4磨成粉末,加入水中制成悬浊液,则所得分散系中分散质粒子直径 10-7m(填“>”或“<”)。
②向CaSO4悬浊液中通入气体时,需先通入足量NH3再通入CO2,原因是 。
某合作学习小组的同学拟用硼砂制取硼酸并测定硼酸样品的纯度。制备硼酸的实验流程如下:
(1)溶解硼砂时需要的玻璃仪器有:烧杯和。
(2)用pH试纸测定溶液pH的操作方法为。
(3)用盐酸酸化硼砂溶液生成硼酸的离子方程式为。
(4)实验流程中缺少的步骤a、步骤b操作分别为、。
(5)硼酸酸性太弱不能用碱的标准溶液直接滴定,实验室常采用间接滴定法,其原理为:
滴定步骤为:
①定到终点时溶液颜色变化是。
②若滴定到终点时消耗NaOH标准溶液22.00mL,则本次滴定测得的硼酸样品中硼酸的质量分数为(假定杂质不反应)。
③若滴定时滴定管尖嘴部分有气泡,滴定过程中消失,将导致测得的结果(选填:“偏大”、“偏小”或“不变”)。
Co2(OH)2CO3和Co(CH3COO)2·nH2O均是生产高比能锂电池正极材料的前驱体。
(1)这两种钴的化合物中钴的化合价为。
(2)Co2(OH)2CO3在空气中充分加热生成四氧化三钴,该反应的化学方程式为。
(3)为确定Co(CH3COO)2·nH2O中的n值及其热分解过程,取一定量的样品在氮气氛围中加热,样品的固体残留率( )随温度的变化如下图所示(样品在300℃前失去结晶水,图中A、B、C、D各处固体均为纯净物,其中C、D为氧化物)。
)随温度的变化如下图所示(样品在300℃前失去结晶水,图中A、B、C、D各处固体均为纯净物,其中C、D为氧化物)。
①Co(CH3COO)2·nH2O晶体中n=(填自然数)。
②A→B点反应释放的气体为纯净物(由两种元素组成),该气体的结构简式为。
③B→C点反应释放CO、CO2两种气体,n(CO)∶n(CO2)=。
④D点残留固体的化学式为。(列出上述计算过程)
长托宁是一种选择性抗胆碱药,可通过以下方法合成(部分反应条件略去):
(1)长托宁中的含氧官能团为_________和_________(填名称)
(2)反应②中加入试剂X的分子式为C8H6O3 ,X的结构简式为_________
(3)反应③的反应类型为_______________
(4)S的同分异构体满足下列条件:
①.能与FeCl3溶液发生显色反应。
②.核磁共振氢谱有5个峰且峰的面积比为2:4:4:1:1;分子中含有两个苯环。写出该同分异构体的结构简式_________________
(5)根据已有知识并结合相关信息,写出以 和
和 为原料制备
为原料制备 的合成路线流程图(无机试剂任用)。合成路线流程图示例如下:
的合成路线流程图(无机试剂任用)。合成路线流程图示例如下:
实验室用辉铜矿(主要成分为Cu2S,含少量Fe2O3、SiO2等杂质)制备碱式碳酸铜的主要实验流程如下。
(1)滤渣Ⅰ的成分为MnO2、单质S和(写化学式);硫酸浸取时,Cu2S被MnO2氧化的化学方程式为。
(2)浸取时,Fe2O3溶于硫酸的离子方程式为;研究发现若先除铁再浸取,浸取速率明显变慢,其可能原因是。
(3)“赶氨”时,最适宜的操作方法是。
(4)滤液Ⅱ经蒸发结晶得到的盐主要是(写化学式)。
(4分)某温度下,在2 L密闭容器中,x、y、z三种物质的物质的量随时间变化曲线如图所示,
由图分析:
(1)该反应的化学方程式是_________________。
(2)3 min末,用y的浓度变化表示的反应速率V(y)为___________。
(3)反应是由_____________开始的反应。
A.正反应 B.逆反应 C.正、逆反应同时