在一定条件下将1mol的CO和水蒸气放入密闭容器中发生反应:CO(g)+H2O(g)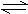 CO2(g)+H2(g),达到平衡时测得CO2为 0.6mol,再通入4mol水蒸气,达到平衡后,CO2的物质的量为 ( )
CO2(g)+H2(g),达到平衡时测得CO2为 0.6mol,再通入4mol水蒸气,达到平衡后,CO2的物质的量为 ( )
| A.0.6mol | B.1mol | C.大于0.6mol小于1mol | D.大于1mol |
下列说法正确的是(NA表示阿伏加德罗常数的值)
| A.28g氮气所含有的原子数目为NA |
| B.在常温常压下,11.2L N2含有的分子数为0.5NA |
| C.0.5mol 单质铝与足量盐酸反应转移电子数为1.5NA |
D.标准状况下,1L水所含分子数为 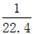 NA NA |
下列反应中,不属于四种基本反应类型,但属于氧化还原反应的是
| A.2Na + 2H2O =" 2NaOH" + H2↑ |
| B.CH4 + 2O2 =CO2 +2H2O |
| C.2KClO3 =" 2KCl" + 3O2↑ |
| D.CaCO3+2HCl = CaCl2+H2O+CO2↑ |
下列状态的物质,既能导电又属于电解质的是
| A.MgCl2固体 | B.NaCl溶液 | C.液体HCl | D.熔融的KOH |
氧化还原反应的实质是
| A.氧元素的得失 | B.化合价的升降 |
| C.电子的得失或偏移 | D.分子中原子的重新组合 |
学习化学过程中需要经常做实验,下列实验操作正确的是
| A.闻气味 | B.倾倒液体 | C.取粉末 | D.过滤 |