下列推论正确的是 ( )
| A.S(s)+O2(g)=SO2(g) △H1, S(g)+O2(g)=SO2(g) △H2;则:△H1<△H2 |
| B.C(石墨,s)=C(金刚石,s)△H=+1.9kJ/mol,则:由石墨制取金刚石的反应是吸热反应,金刚石比石墨稳定 |
| C.NaOH(aq)+HCl(aq)=NaCl(aq)+H2O(l) △H= —57.4kJ/mol,则:含20gNaOH的溶液与稀盐酸完全反应,放出的热量为28.7kJ |
| D.CaCO3(s)=CaO(s)+CO2(g) △H>0,△S>0,则:该反应任何温度下都能自发进行 |
标准状况下V L氨气溶解在1 L水中(水的密度近似为1 g·mL-1),所得溶液的密度为ρ g·mL-1,质量分数为w,物质的量浓度为c mol·L-1,则下列关系中不正确的是
A.ρ=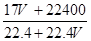 |
B.w=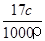 |
C.w= |
D.c=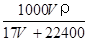 |
NA为阿伏加德罗常数的值。下列说法正确的是
| A.18gD2O和18gH2O中含有的质子数均为10NA |
| B.2 L 0.5mol/L亚硫酸溶液中含有的H+离子数为2NA |
| C.过氧化钠与水反应时,生成0.1mol氧气转移的电子数为0.2NA |
| D.密闭容器中2mol NO与1mol O2充分反应,产物的分子数为2NA |
将0.195g锌粉加入到20.0mL的0.100 mol·L-1MO2+溶液中,恰好完全反应,则还原产物可能是
| A.M | B.M3+ | C.M2+ | D.MO2+ |
已知在碱性溶液中可发生如下反应:2R(OH)3+3ClO﹣+4OH﹣═2RO4n﹣+3Cl﹣+5H2O,则RO4n﹣中R的化合价是
| A.+3 | B.+4 | C.+5 | D.+6 |
根据表中信息判断,下列选项正确的是
| 序号 |
反应物 |
产物 |
| ① |
KMnO4、H2O2、H2SO4 |
K2SO4、MnSO4… |
| ② |
Cl2、FeBr2 |
FeCl3、FeBr3 |
| ③ |
MnO4﹣… |
Cl2、Mn2+… |
A.第①组反应的其余产物只有O2
B.第②组反应中Cl2与FeBr2的物质的量之比为1:2
C.第③组反应中生成1molCl2,转移电子10mol
D.氧化性由强到弱顺序为MnO4﹣>Cl2>Fe3+>Br2