框图中A是人体胃液中含有的成分,B用于改良酸性土壤,G是铁锈的主要成分(Fe2O3·xH2O),E、F、I为无色气体。根据图示回答下列问题。
(1)写出有关物质的化学式:B : ,C: 。
(2)写出反应④的化 学方程式: 。
学方程式: 。
(3)反应①属于 反应(填反应类型)。
(4)日常生活中为了阻止反应③发生,通常采取的措施是 (写一条)。
(5)要使反应⑤能够发生,需要反应物B和M,其中M的化学式为 。
A、B、C、D、E都是初中化学中常见的化合物,其中A为白色固体,B为无色气体,E为不溶于稀硝酸的白色沉淀,它们的关系如下图所示.(该实验条件下,如果涉及微溶物质,视为可溶)
回答下列问题:
(1)若现象I为“生成白色沉淀”,则反应①的化学方程式为 ;
②的化学方程式为 。
(2)若现象I为“无明显变化”,则A的化学式可能为 等。
A、B、C、D是初中阶段常见的物质,其中A是一种无色液体,它们之间的相互转化如下图所示。试判断:
(1)写出A在空气中燃烧的化学方程式;
(2)B、D两种物质可以相互转化,请分别写出一种转化的方法:

下图所示的是有关物质相互转化的关系图,其中A是一种金属氧化物,G是红褐色沉淀,I 的溶液呈浅绿色。
根据关系图回答:
(1)若F是由Na+和Cl—组成的溶液,则:①甲是;
②B+丙→F+G:。
(2)若D是能使澄清石灰水变浑浊的气体,则:①乙可能是或;
②I是溶液。
(3)若乙是具有还原性的气体单质,写出A与乙反应的化学方程式
A—I为初中化学中常见的物质。已知A为金属氧化物,C为大理石的主要成分,D为蓝色沉淀,G、I均为只含有一种溶质的溶液。“→”表示物质间存在着相互转化的关系(部分生成物未标出),如下图所示。请回答下列问题: 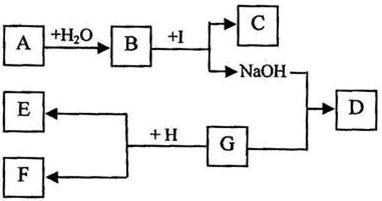
(1)写出化学式:A,D。
(2)写出B与I 反应的化学方程式:。
(3)已知H为一定量锌粉和铁粉的混合物,与溶液G充分反应后过滤。向滤渣E中加入稀盐酸,有无色气体放出,则滤渣E中一定含有,滤液F中一定含有的金属阳离子是。
a、b、c、d、e为初中常见的五种化合物,它们的水溶液相互反应关系如下:
①a+b→c+H2O②c+H2SO4→d+a③e+AgNO3→AgCl+c,
(1)则a、c的化学式分别是:a:;c:。
(2)写出②的化学方程式为;
(3)请写出一个“有水生成不一定是中和反应”这个观点的化学方程式:
。