在常温下,Fe与水并不起反应,但在高温下,Fe与水蒸气可发生反应。 应用下列装置,在硬质玻璃管中放入还原铁粉和石棉绒的混合物,加热,并通入水蒸气,就可以完成高温下“Fe与水蒸气的反应实验”。
请回答该实验中的问题。
(1)写出该反应的反应方程式: ;并指明该氧化还原反应 的还原剂是 ,氧化剂是 。
的还原剂是 ,氧化剂是 。
(2)实验前必须对整套装置进行气密性检查,操作方法是 。
(3)试管中收集气体是  ,如果要在A处玻璃管处点燃该气体,则必须对该气体进行 ,方法是 。这一操作的目的是
,如果要在A处玻璃管处点燃该气体,则必须对该气体进行 ,方法是 。这一操作的目的是  。
。
(15分)高铁酸钾(K2FeO4)是一种集氧化、吸附、速凝于一体的新型多功能水处理剂。其生产流程如下:

(1)配制KOH溶液时,是在每100 mL水中溶解61.6 g KOH固体(该溶液的密度为1.47 g/mL),它的物质的量浓度是 mol/L。
(2)在溶液I中加入KOH固体的目的是 (填编号)。
| A.与溶液I中过量的Cl2继续反应,生成更多的KclO |
| B.KOH固体溶解时会放出较多的热量,有利于提高反应速率 |
| C.为下一步反应提供碱性的环境 |
| D.使副产物KClO3转化为 KClO |
(3)每制得59.4克K2FeO4,理论上消耗氧化剂的物质的量为 mol。从溶液II中分离出K2FeO4后,还得到副产品KNO3、KCl,写出③中反应的离子方程式: 。
(4)高铁酸钾(K2FeO4)溶液中加入稀硫酸,溶液变为黄色,并有无色气体产生,该反应的离子方程式是 。
(5)从环境保护的角度看,制备K2FeO4较好的方法为电解法,其装置如图2所示。电解过程中阳极的电极反应式为 。
某实验小组利用如下装置合成化工原料正丁醛。发生的反应如下: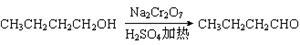
反应物和产物的相关数据列表如下:
| 沸点/℃ |
密度/(g·cm-3) |
水中溶解性 |
|
| 正丁醇 |
117.2 |
0.810 9 |
微溶 |
| 正丁醛 |
75.7 |
0.801 7 |
微溶 |
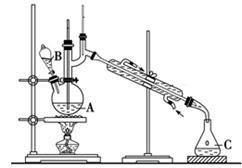
实验步骤如下:
将6.0 g Na2Cr2O7放入100 mL烧杯中,加30 mL水溶解,再缓慢加入5 mL浓硫酸,将所得溶液小心转移至B中。在A中加入4.0 g正丁醇和几粒沸石,加热。当有蒸气出现时,开始滴加B中溶液。滴加过程中保持反应温度为90~95 ℃,在C中收集90 ℃以下的馏分。将馏出物倒入分液漏斗中,分去水层,再将有机层干燥、蒸馏后得正丁醛2.0 g。
回答下列问题:
(1)实验中不能将Na2Cr2O7溶液加到浓硫酸中的理由是 。
(2)加入沸石的作用是 。
(3)分液漏斗使用前必须进行的操作是 。
(4)反应温度应保持在90~95℃,其原因是 。
(5)本实验中,正丁醛的产率为 。
(13分)以下是实验室常用的部分仪器。
请回答下列问题:
(1)序号为⑧和⑩的仪器分别为 、 (填名称、下同)。
(2)能作反应容器且可直接加热的是 。
(3)在分液操作中,必须用到仪器是 (填序号、下同)。
(4)在配制一定物质的量浓度的溶液时,需要上述仪器中的 。
(5)仪器上标有温度的是 。
(6)下图是温度计、量筒、滴定管的一部分,下述读数(虚线刻度)及说法正确的是________。
a.①是量筒,读数为2.5 mL
b.②是量筒,读数为2.5 mL
c.③是滴定管,读数为2.5 mL
d.②是温度计,读数是2.5 ℃
(7)某同学想用大理石和稀盐酸反应制取少量CO2。教师指出,若用下列装置制取会浪费大量的稀盐酸。于是该同学选用了上述①~⑩中的一种仪器,添加在下列装置中,解决了这个问题。请你将需要添加的仪器画在下图中的合适位置。
己知氨可以与灼热的氧化铜反应得到氮气和金属铜,用示意图中的装置可以实现该反应。
回答下列问题:
(1)A中生成氨气反应的化学方程式是 _________________;
(2)B中加入的干燥剂是_______(填序号)①浓硫酸②无水氯化钙③碱石灰;
(3)能证明氨与氧化铜反应的现象:①C中______、②D中有无色液体生成;
设计实验检验D中无色液含有水:取少量液体于试管中,加入少量_______粉末,现象为______。
(4)写出氨气与氧化铜反应的化学方程式 _______________。若收集到2.24L(STP)氮气,计算转移电子数为______________。
下图是实验室中制备气体或验证气体性质的装置图
(1)写出用发生装置A中制取氯气的化学方程式______________。
(2)利用上图装置制备纯净的氯气,并证明氧化性:C12>Fe3+,则装置B中的溶液的作用是______;装置D中加的最佳试剂是(填序号)_________________:
供选试剂:a.浓H2SO4 b.FeCl2溶液 c.KSCN与FeCl2的混合溶液 d.无水氯化钙
(3)在上图所示圆底烧瓶内加入碳,a中加入浓硫酸,开始实验,加热产生的气体缓慢通过后续装置同时完成如下实验:
实验1:证明SO2具有氧化性和漂白性
实验2:证明碳元素的非金属性比硅元素的强
证明SO2具氧化性和漂白性:B中为少量Na2S溶液、C中加品红溶液,D中应加入足量的___________(填溶液名称),E中加入___________溶液(填化学式)。
(4)证明碳元素的非金属性比硅元素的强的现象为_________;实验2不严谨之处应如何改进________。