(11分)(1)在同一个原子中,离核越近、n越小的能层中的电子能量越 。理论研究证明,多电子原 子中,同一能层的电子,能量也可能不同,还可以把它们分成能级,第三能层有3个能级,分别为3s、3p和 。现代物质结构理论证实,原子的电子排布遵循构造原理能使整个原子的能量处于最低状态,处于最低能量的原子叫做 原子。
子中,同一能层的电子,能量也可能不同,还可以把它们分成能级,第三能层有3个能级,分别为3s、3p和 。现代物质结构理论证实,原子的电子排布遵循构造原理能使整个原子的能量处于最低状态,处于最低能量的原子叫做 原子。
(2) N≡N的键能为946kJ·mol-1,N—N单键的键能为193kJ·mol-1,计算说明N2中的 键更稳定(填“σ”或“π”)。
(3)在配离子[Fe(SCN)]2+中,提供空轨道接受孤电子对的微粒是 ,配离子 [Cu(NH3)4]2+的配体是 。
(4)根据价层电子对互斥理论判断下列问题:
①NH3中心原子的杂化方式为 杂化,VSEPR构型为 ,分子的立体构型为 。
②BF3分子中,中心原子的杂化方式为 杂化,分子的立体构型为 。
现有如下两个反应:(A)NaOH + HCl =" NaCl" + H2O
(B)2FeCl3 + Cu = 2FeCl2 + CuCl2
(1)根据两反应本质,判断能否设计成原电池A:, B:______(填“能”与“不能”)
如果不能,说明其原因
(2)根据能设计成原电池的反应选择适宜的材料和试剂设计一个原电池:
①负极材料是, 正极材料是_______,电解质溶液是;
②写出正极的电极反应式,正极发生反应(填“氧化”或“还原”),
③若导线上转移电子0.1mol,则负极质量变化克。
除去下列物质中的杂质,根据要求填空:
| 物质 |
杂质 |
选用试剂 |
离子方程式 |
| FeCl2溶液 |
FeCl3 |
||
| SiO2 |
Al 2O3 |
||
| Fe2O3 |
Al 2O3 |
按要求用合适的化学用语填空
Ⅰ.在原子序数1—18号元素中:
(1)与水反应最剧烈的金属是_____________。
(2)与水反应最剧烈的非金属单质是_____________。
(3)原子半径最小的元素是_____________。
(4)气态氢化物最稳定的化学式是_____________。
(5)电子数为10的分子(写5个)
Ⅱ.下列各分子中,所有原子都满足最外层为8电子结构的是
①. H2O②. BF3③.CCl4④. PCl3⑤. SO3⑥. N2⑦. CO2
为扩大现有资源的使用效率,在一些油品中加入降凝剂J,以降低其凝固点,扩大燃料油品的使用范围。J是高分子聚合物,它的合成线路可以设计如下,其中A的氧化产物不发生银镜反应:
试写出:
(1)反应类型:abc
(2)结构简式:FH
(3)化学方程式:D→E
E+K→J
三种常见元素结构信息如下表,试根据信息回答有关问题:
| 元素 |
A |
B |
C |
| 结构信息 |
基态原子核外有两个电子层,最外层有3个未成对的电子 |
基态原子的M层有1对成对的p电子 |
基态原子核外电子排布为[Ar]3s104sx,有+1、+ 2两种常见化合价 2两种常见化合价 |
(1)写出B原子的基态电子排布式;
(2)用氢键表示式写出A的氢化物溶液中存在的氢键(任写一种);A的氢化物分子结合一个H+形成阳离子后,其键角(填写“变大”、“变小”、“不变”);
(3)往C元素的硫酸盐溶液中逐滴加入过量A元素的氢化物水溶液,可生成的配合物的化学式为,简要描述该配合物中化学键的成键情况;
(4)下列分子结构图中的“●”表示上述相关元素的原子中除去最外层电子的剩余部分,“○”表示氢原子,小黑点“·”表示没有形成共价键的最外层电子,短线表示共价键。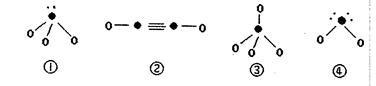
在以上分子中,中心原子采用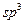 杂化形成化学键是(填写序号);在②的分子中有个
杂化形成化学键是(填写序号);在②的分子中有个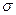 键和个
键和个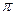 键。
键。