在标准状况下,m g A气体与n g B气体分子数相等,下列说法不正确的是( )
| A.标准状况下,同体积的气体A和气体B的质量比m : n |
| B.25 ℃时,1 kg气体A与1 kg气体B的分子数之比为n : m |
| C.同温同压下,气体A与气体B的密度之比为m : n |
| D.标准状况下,等质量的A与B的体积比为m : n |
下列化学式只能表示一种物质的是
| A. P | B. C4H10 | C. C2H4Cl2 | D. CH2Cl2 |
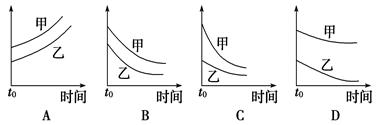
下列表格中的各种情况,可以用下面对应选项中的图象曲线表示的是
| 选项 |
反应 |
纵坐标 |
甲 |
乙 |
| A |
外形、大小相近的金属和水反应 |
反应速率 |
Mg] |
Na |
| B |
4 mL 0.01 mol/L的KMnO4溶液,分别和不同浓度的H2C2O4(草酸)溶液各2mL反应 |
0.1 mol/L的H2C2O4溶液 |
0.2 mol/L的H2C2O4溶液 |
|
| C |
5 mL 0.1 mol/L Na2S2O3溶液和5 mL 0.1 mol/L H2SO4溶液反应 |
热水 |
冷水 |
|
| D |
5 mL 4%的过氧化氢溶液分解放出O2 |
无MnO2粉末 |
加MnO2粉末 |
在mA(气)+nB(气)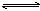 pC(气)+qD(气)反应中,经10min达平衡,此时各物质的浓度变化为:A减少amol/L,B减少a/3 mol/L,C增加2a/3 mol/L,此时若给体系加压,化学平衡不移动,则m:n:p:q为
pC(气)+qD(气)反应中,经10min达平衡,此时各物质的浓度变化为:A减少amol/L,B减少a/3 mol/L,C增加2a/3 mol/L,此时若给体系加压,化学平衡不移动,则m:n:p:q为
| A.1:1:1:1 | B.1:3:3:1 |
| C.1:3:2:2 | D.3:1:2:2 |
可逆反应2SO2(g)+O2(g) 2SO3(g),△H<0。在一定条件下达到平衡状态,时间为t1时改变条件,反应速率与时间关系如图,下列说法正确的是
2SO3(g),△H<0。在一定条件下达到平衡状态,时间为t1时改变条件,反应速率与时间关系如图,下列说法正确的是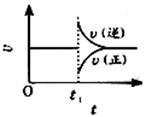
| A.维持温度与容积不变,t1时充入SO3(g) |
| B.维持压强不变,t1时升高温度 |
| C.维持温度不变,t1时扩大容积 |
| D.维持温度和压强不变,t1时充入SO3(g) |
可逆反应a A(s)+b B(g) c C(g)+d D(g),反应过程中,当其它条件不变时,C的百分含量(C%)与温度(T)和压强(P)的关系如图,下列叙述正确的是:
c C(g)+d D(g),反应过程中,当其它条件不变时,C的百分含量(C%)与温度(T)和压强(P)的关系如图,下列叙述正确的是:
| A.达到平衡后,加入催化剂则C%增大 |
| B.达到平衡后,若升高温度,平衡向右移动 |
| C.化学方程式中b < c +d |
| D.达平衡后,增加A的量,有利于平衡向右移动 |