设NA表示阿伏加德罗常数,下列说法正确的是
| A.1 mol氯气参加氧化还原反应,转移的电子数一定为2NA |
| B.标准状况下,以任意比混合的氢气和一氧化碳气体共8.96 L,在足量氧气中充分燃烧时消耗氧气的分子数为0.2NA |
| C.含1 mol FeCl3的溶液中Fe3+的个数为NA |
| D.1.8 g NH4+中含有的电子数为0.1NA |
下列关于盐酸和醋酸两种稀溶液的说法正确的是()
| A.相同浓度的两溶液中c(H+)相同 |
| B.100 mL 0.1 mol·L-1的两溶液能中和等物质的量的氢氧化钠 |
| C.pH=3的两溶液稀释100倍,pH都为5 |
| D.两溶液中分别加入少量对应的钠盐,c(H+)均明显减小 |
对水的电离平衡不产生影响的粒子是()
| A.HCl | B.CH3COO- | C.Fe3+ | D.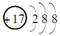 |
在2A+B===3C+4D的反应中,下列表示该反应的化学反应速度最快的是()
A.v(A)=0.5 mol·L-1·s-1
B.v(B)=0.3 mol·L-1·s-1
C.v(C)=0.8 mol·L-1·s-1
D.v(D)=1.0 mol·L-1·s-1
下列叙述中,能证明某物质是弱电解质的是()
| A.熔化时不导电 |
| B.不是离子化合物,而是极性共价化合物 |
| C.水溶液的导电能力很差 |
| D.溶液中已电离出的离子和未电离的分子共存 |
我国第五套人民币中的一元硬币材料为钢芯镀镍,依据你所掌握的电镀原理,你认为硬币制作时,钢芯应该做()
| A.正极 | B.负极 |
| C.阳极 | D.阴极 |