从海水中可以提取镁,其中的一个步骤是将卤水(含
、
、
的混合液)转化为氯化镁晶体。实验室中模拟该转化的过程如下,回答有关问题a
(1)制备氢氧化镁:向卤水中加入适量生石灰(
),充分反应后过滤。
①该过程中发生了多个反应,其中会大量放热的反应是(填化学方程式)②过滤操作需用到的玻璃仪器除烧杯外,还有。
(2)制各氯化镁溶液:用盐酸溶解
。为了便于后续操作.盐酸不宜过量
①反应的化学方程式是。
②通过计算,可准确知道所需盐酸的量。理论上溶解5.8
需要36. 5
HCl溶液
③由于准确称量
的步骤繁琐,实验中并不常用,而是通过一定操作方法来达到
到控制盐酸用量的目的。操作是:将
加入烧杯中,直到
完全溶解为止。
(3)制各氯化镁晶体:蒸发浓缩
溶液,冷却结晶
清华大学研究人员成功研制出一种纳米纤维催化剂,可将二氧化碳转化成液体燃料甲醇,其微观示意图如图(图中的微粒恰好完全反应)。请回答下列问题。

(1)丁的化学式为
(2)参加反应的甲、乙两物质的质量比为 。(填最简整数比)
(3)由该图可知,分子和原子的本质区别是 。
十九大报告对于"精准扶贫"做出了总体安排。脱贫先治水,让贫困地区喝上干净安全的自来水是脱贫的基本要求。
(1)自来水的生产过程中,常用活性炭去除水中异味,这是利用活性炭的 性。
(2)有些村民用地下水作生活用水,人们常用 检验地下水是硬水还是软水,生活中可用的 方法降低水的硬度。
(3)下列做法会造成水体污染的是
①不向河中扔垃圾
②生活污水直接排放
③工业废水直接排放
④农业上合理使用农药、化肥
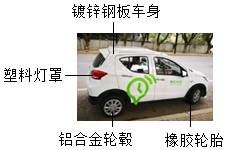
继"共享单车"之后又推出了"共享汽车"。如图所示,"共享汽车"使用的是纯电动汽车,充满电时可行驶约170公里。请回答下列问题。
(1)"共享汽车"的外部材料中属于有机合成材料的是 (填一种即可);属于金属材料的是 (填一种即可)。
(2)电动汽车的使用减少了化石燃料的消耗,同时,汽车与传统燃油汽车相比,还具有的主要优点是
(3)请用分子的观点解释"炎热的夏天,自行车轮胎易爆胎"的原因 。
将下列短文中带点的部分,用恰当的化学用语填空。
大约46亿年前地球形成时,温度很高,大气主要含氦元素和氢元素 ,随着地球的冷却,大气中的水蒸气冷凝并以雨水的形式降落到地表,氯化钠(氯化钠中钠元素的化合价显+1价 )、铵盐(铵根离子 )等盐溶于雨水,雨水充满了地表,海洋由此形成。
你中午吃西瓜了吗?下表列出的是某品种西瓜每100g食用部分的主要营养成分数据。
|
营养成分 |
水分 |
蛋白质 |
脂肪 |
糖类 |
X |
钙铁锌 |
|
质量 |
92.5g |
0.7g |
0.2g |
6.1g |
6.8mg |
17.1mg |
(1)表中"X"是指人体所需六大基本营养素中的 ,其作用是 。
(2)西瓜中含有的 元素可预防贫血。