氢化亚铜(CuH)是一种难溶物质,用CuSO4溶液和“另一物质”在40~50℃时反应可生成它.CuH具有的性质有:不稳定,易分解;在氯气中能燃烧;与稀盐酸反应能生成一种单质气体;Cu+在酸性条件下发生的反应是:2Cu+===Cu2++Cu.
根据以上信息,结合自己所掌握的化学知识,回答下列问题:
(1)用CuSO4溶液和“另一物质”制CuH的反应中,用氧化还原观点分析,这“另一物质”在反应中作________(填“氧化剂”或“还原剂”).
(2)写出CuH在氯气中燃烧的化学反应方程式:_______________________.
(3)CuH溶解在足量稀盐酸中生成的气体是______(填化学式);
该反应的氧化剂是 。(填化学式)
(4)如果把CuH溶解在足量的稀硝酸中生成的气体只有NO,请写出CuH溶解在足量稀硝酸中反应的离子方程式:________________________________________.
化合物A、D、F是中学化学中常见的物质,化合物B、C、E中含有两种相同的元素。
这些化合物之间存在如图的关系。其中A和B的反应是一种重要化工生产中的主要反应之一。请完成下列问题:
(1)在A、C、F中含有相同的元素是__________。
(2)化合物C的化学式是________,化合物A的水溶液显__________性(填“酸”“碱”或“中”)。
(3)C的水溶液与D能否发生反应?________,理由是____________________。
氮化硅是一种高温陶瓷材料,它的硬度大、熔点高、化学性质稳定,工业上曾普遍采用高纯硅与纯氮在1 300 ℃反应获得。
(1)写出N原子结构示意图:_______,根据元素周期律知识,请写出氮化硅的化学式:_______。
(2)氮化硅陶瓷抗腐蚀能力强,除氢氟酸外,它不与其他无机酸反应。试推测该陶瓷被氢氟酸腐蚀的化学方程式:______________。
(3)现用四氯化硅和氮气在氢气气氛保护下,加强热发生反应,可得较高纯度的氮化硅,反应的化学方程式为______________。
根据下图所示的物质之间的转化关系,其中A为单质,回答下列有关问题。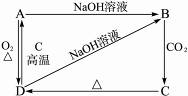
(1)写出A、B、C、D各物质的名称:
A,B,
C,D。
(2)写出下列变化的化学方程式:
D→A;
B→C;
D→B。
某型号的水泥主要成分有Ca2SiOx、Ca3SiOy、Ca3Al2Oz,则x=,y=,z=。
水泥具有水硬性,跟水掺和搅拌后很容易,水泥要保存。
普通水泥以和为主要原料,煅烧后再加入适量,用以调节硬化速度。
用高岭土(主要成分是Al2O3·2SiO2·2H2O,并含有少量CaO、Fe2O3)研制新型净水剂(铝的化合物)。其步骤如下:将土样和纯碱混合均匀,加热熔融,冷却后加盐酸分别得到沉淀和溶液,溶液即为净水剂。
(1)写出熔融时主要成分与纯碱反应的化学方程式(Al2O3与强碱反应相似)。
(2)最后的沉淀是,生成沉淀的离子方程式是。
(3)实验室中常用的有瓷坩埚、氧化铝坩埚和铁坩埚,本实验应选用坩埚。