工业盐中含有NaNO2,外观和食盐相似,有咸味,人若误食会引起中毒,致死量为0.3g~0.5g。已知NaNO2能发生如下反应:2NO + xI-+ yH+ = 2NO↑+ I2 + zH2O,请回答下列问题:
+ xI-+ yH+ = 2NO↑+ I2 + zH2O,请回答下列问题:
(1)上述反应中,x的数值是 ,y的数值是 。
(2)根据上述反应,可用化学试纸及生活中常见物质进行实验来鉴别工业盐和食盐,
现有碘化钾淀粉试纸,则还需选用的生活中常见物质的名称为 。
(3)某工厂废切削液中含有2%—5%的NaNO2,直接排放会造成水污染,但加入下
列物质中的某一种就能使NaNO2转化为不引起污染的N2,该物质是 ,
a.NaCl b.H2O2 c.NH4Cl d.浓H2SO4
所发生反应的离子方程式为:
用大试管收集一试管NO2气体,倒扣在盛水的水槽里,试管内产生的现象为;再往试管里通入适量氧气,试管内又产生的现象为。产生上述现象的原因是
工业上常用铁质容器盛装冷浓硫酸。为研究铁质材料与热浓硫酸的反应,某学习小组进行了以下探究活动:
(1)将已去除表面氧化物的铁钉(碳素钢)放入冷浓硫酸中,10分钟后移入硫酸铜溶液中,片刻后取出观察,铁钉表面无明显变化,其原因是__________ ______________________________________。
(2)另称取铁钉6.0g放入15.0ml浓硫酸中,加热,充分应后得到溶液X并收集到气体Y。
①甲同学认为X中除Fe3+外还可能含有Fe2+。写出生成Fe2+所有可能的离子反应方程式:。
若要确认其中有Fe2+,应选用(选填序号)。
a.KSCN溶液和氯水 b.铁粉和KSCN溶液
c.浓氨水 d.酸性KMnO4溶液
②乙同学取336ml(标准状况)气体Y通入足量溴水中,发生反应的化学方程式为:。
然后加入足量BaCl2溶液,经适当操作后得干燥固体2.33g。由于此推知气体Y中SO2的体积分数为。
已知有以下物质相互转化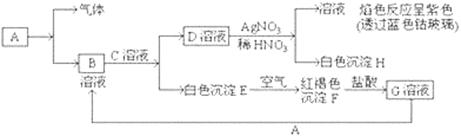
试回答:(1)写出E的化学式,H的化学式。
(2)写出由E转变成F的化学方程式。
(3)检验G溶液中的金属阳离子的方法是:;
向G溶液加入A的有关离子反应方程式。
(4)写出A在一定条件下与水反应的化学方程式。
如下图所示中各方框表示有关的一种反应物或生成物(某些物质已经略去),其中常温下A、C和D为无色气体,C能使湿润的红色石蕊试纸变蓝,X分解产生A、B和C三种产物的比值为1:1:1。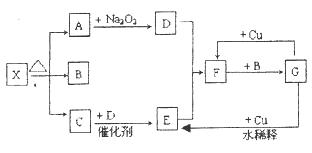
(1)写出下列各物质的化学式:
X:;B:;F:;G:。
(2)按要求写出下列变化的反应化学方程式:
A→D的化学反应方程式:;
G→E的离子反应方程式:。
把19.2 g 的Cu放入500mL 2 mol·L-1稀硝酸中,充分反应,Cu完全溶解。求:
(1)写出Cu与稀硝酸反应的离子方程式:;
(2)铜完全溶解时转移电子数目为(用含NA的式子表示);
(3)氧化剂与还原剂的物质的量比为。
(4)反应后溶液中C(H+)为(体积变化忽略不计)