.以富含硫酸亚铁的工业废液为原料生产氧化铁的工艺如下(部分操作和条件略):
Ⅰ.从废液中提纯并结晶出FeSO4·7 H2O。
H2O。
Ⅱ.将FeSO4·7H2O配制成溶液。
Ⅲ.FeSO4溶液与稍过量的NH4HCO3溶液混合,得到含FeCO3的浊液。
Ⅳ.将浊液过滤,用90 ℃热水洗涤沉淀,干燥后得到FeCO3固体。
Ⅴ.煅烧FeCO3,得到Fe2O3固体。
已知:NH4HCO3在热水中分解。
(1)Ⅰ中,加足量的铁屑除去废液中的Fe3+,该反应的离子方程式是_________________。
(2)Ⅱ中,需加一定量酸,该酸最好是 。运用化学平衡原理简述该酸的作用________________________________________________________________________。
(3)Ⅲ中,生成FeCO3的离子方程式是___________________________________________
若FeCO3浊液长时间暴露在空气中,会有部分固体表面变为红褐色,该变化的化学方程式是_______________________________________。
(4)Ⅳ中,通过检验SO来判断沉淀是否洗涤干净,检验SO的操作是__________
________________________________________________________________________。
(5)已知煅烧FeCO3的化学方程式是4FeCO3+O22Fe2O3+4CO2。现煅烧464.0  kg的FeCO3,得到316.8 kg产品。若产品中杂质只有FeO,则该产品中Fe2O3的质量是________kg。(摩尔质量/g·mol-1:FeCO3 116 Fe2O3 160 FeO 72)
kg的FeCO3,得到316.8 kg产品。若产品中杂质只有FeO,则该产品中Fe2O3的质量是________kg。(摩尔质量/g·mol-1:FeCO3 116 Fe2O3 160 FeO 72)
(8分)请同学们根据官能团的不同对下列有机物进行分类。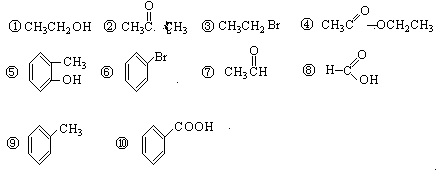
(1)芳香烃:;(2)卤代烃:;(3)醇:;(4)酚:;
(5)醛:;(6)酮:;(7)羧酸:;(8)酯:。
(10分)汽车尾气里含有的NO气体是由于内燃机燃烧的高温引起氮气和氧气反应所致:N2(g)+O2(g) 2NO(g),ΔH>0,已知该反应在2 404℃,平衡常数K=64×10-4。请回答:
2NO(g),ΔH>0,已知该反应在2 404℃,平衡常数K=64×10-4。请回答:
(1)某温度下,向2 L的密闭容器中充入N2和O2各1 mol,5分钟后O2的物质的量为0.5 mol,则N2的反应速率为_____________________。
(2)为了减少汽车尾气中有害气体的排放,在现实生活中你认为可以采取的措施有。
| A.采用耐高温的陶瓷发动机,以提高内燃机的工作温度 |
| B.为了避免上述反应,不使用空气,改用纯氧气 |
| C.在排气管中安装高效催化剂,将有害气体转化为无害气体 |
| D.将燃油车改换成电动车 |
(3)将一定量的N2、O2的混合气体充入恒容密闭容器中,下图变化趋势正确的是____________(填字母序号)。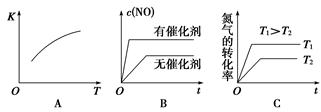
(4)将一定量的N2、O2的混合气体充入恒温密闭容器中,分别在不同的压强P1、P2(P1>P2)下达到平衡,请画出N2的转化率在不同压强下随时间变化的曲线图。(不同压强下的曲线要有相应的标识)
(1)已知下列各反应的焓变
①Ca(s)+C(s,石墨)+3/2O2(g)=CaCO3(s)△H1 = -1206.8 kJ/mol
②Ca(s)+1/2O2(g)=CaO(s)△H2= -635.1 kJ/mol
③C(s,石墨)+O2(g)=CO2(g)△H3 = -393.5 kJ/mol
试求:④CaCO3(s)=CaO(s)+CO2(g)△H=________。
(2)已知下列各反应的焓变
①CO(g)+1/2O2(g)=CO2(g) ΔH1= -283.0 kJ/mol
②H2(g)+1/2O2(g)=H2O(l) ΔH2= -285.8 kJ/mol
③C2H5OH(l)+ 3O2(g)=2CO2(g)+3H2O(l) ΔH3=-1370 kJ/mol
试求:④2CO(g)+4H2(g)=H2O(l)+C2H5OH(l) ΔH=________。
(8分)能源问题是人类社会面临的重大课题,甲醇是未来重要的能源物质。一定条件下,在体积为2 L的密闭容器中,1mol一氧化碳与2mol氢气反应生成甲醇(催化剂为Cu2O/ZnO):
CO(g)+2H2(g) CH3OH(g)△H<0
CH3OH(g)△H<0
根据题意完成下列各题:
反应达到平衡时,平衡常数表达式K=,升高温度,K值(填“增大”、“减小”或“不变”)。
(2)在500℃,10min反应达平衡,此时甲醇的物质的量浓度为0.3mol/L,从反应开始到平衡,氢气的平均反应速率v(H2)=。
(3)在其它条件不变的情况下,把反应处于平衡体系的容器的体积压缩为1 L,下列有关该体系的说法正确的是。
| A.平衡向正反应方向移动 | B.正反应速率加快,逆反应速率减慢 |
| C.甲醇的物质的量增加 | D.重新平衡时c(CO)/c(CH3OH)不变 |
(12分)(1)已知C(s、金刚石)+O2==CO2(g) ΔH=-395.4kJ/mol,
C(s、石墨)+O2==CO2(g) ΔH=-393.5kJ/mol。
①石墨和金刚石相比,石墨的稳定性金刚石的稳定性。
②石墨中C-C键键能______金刚石中C-C键键能。(均填“大于”、“小于”或“等于”)。
(2)肼(N2H4)和NO2是一种双组分火箭推进剂。两物质混合发生反应生成N2和H2O(g),已知8g气体肼在上述反应中放出142kJ热量,其热化学方程式为:。
(3)0.3mol的气态高能燃料乙硼烷(B2H6)在氧气中燃烧,生成固态三氧化二硼和液态水,放出649.5kJ热量,其热化学反应方程式为:;
又知H2O(l)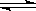 H2O(g),△H=+44kJ/mol,则11.2L(标准状况)乙硼烷完全燃烧生成气态水时,放出的热量是kJ。
H2O(g),△H=+44kJ/mol,则11.2L(标准状况)乙硼烷完全燃烧生成气态水时,放出的热量是kJ。