纳豆是一种减肥食品,从其中分离出一种由C、H、O三种元素组成的有机物A,为确定其结构现进行如下各实验:
①6.0gA在一定条件下完全分解,生成3.36L(标准状况下)一氧化碳和1.8g水;
②中和0.24g物质A消耗0.2mol/L的NaOH溶液20.00mL;
③0.01mol物质A完全转化为酯,需要乙醇0.92g,0.01molA能与足量钠反应放出0.336L(标准状况下)氢气。
通过计算确定:⑴A的摩尔质量是 A的化学式为
⑵A的结构简式是
为了确定CH3COOH、 及H2CO3的酸性强弱,有人设计了如图所示的装置进行实验:
及H2CO3的酸性强弱,有人设计了如图所示的装置进行实验: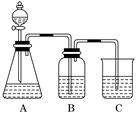
(1)若锥形瓶中装有一种易溶于水的正盐固体,则A中发生反应的离子方程式为________________________________________________________________________.
(2)装置B中盛放的试剂是________,它的作用是___________________________
______________________________________________________________________.
(3)实验中观察到C中出现的主要现象是_________________________________
________________________________________________________________________.
醇和酚在人类生产和生活中扮演着重要的角色,根据醇和酚的概念和性质回答下列问题.
(1)下列物质属于醇类的是________.
①CH3CH2CH2OH
②CH3CH(OH)CH3
③CH2===CH—CH2OH
④CH2OH—CH2OH
(2)司机酒后驾车时可检测他呼出的气体,所利用的化学反应如下:
2CrO3(红色)+3C2H5OH+3H2SO4===Cr2(SO4)3(绿色)+3CH3CHO+6H2O
被检测的气体成分是________,上述反应中的氧化剂是________,还原剂是________.
(3)300多年前,著名化学家波义耳发现了铁盐与没食子酸的显色反应,并由此发明了
蓝黑墨水.没食子酸的结构式为: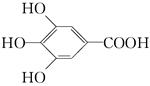 用没食子酸制造墨水主要利用了________类化合物的性质(填代号).
用没食子酸制造墨水主要利用了________类化合物的性质(填代号).
| A.醇 | B.酚 | C.油脂 | D.羧酸 |
把少量的苯酚晶体放入试管中,加入少量水振荡,溶液里出现________,因为__________________________.逐渐滴入稀NaOH溶液,继续振荡,溶液变为________,其离子方程式为__________________________.向澄清的溶液中通入过量CO2,溶液又变为________,其离子方程式为__________________________.
松油醇是一种调味香精,它是α、β、γ三种同分异构体组成的混合物,可由松节油分馏产品A(结构式和H2O中的“18”是为区分2个羟基而人为加上去的)经如图所示反应制得.
试回答:
(1)α松油醇的分子式是________.
(2)α松油醇所属的物质类别是________.
a.醇 b.酚 c.饱和一元醇
(3)α松油醇所能发生的反应类型是________.
a.加成 b.水解 c.氧化
(4)写出结构简式:β松油醇:___________________________________________;
γ松油醇:________________________.
从樟科植物枝叶提取的精油中含有下列甲、乙两种成分:
(1)甲中含氧官能团的名称为________.
(2)由甲转化为乙需经下列过程(已略去各步反应的无关产物):
其中反应Ⅰ的反应类型为________,反应Ⅱ的化学方程式为____________________(注明反应条件).