根据下列反应判断有关物质还原性由强到弱的顺序是( )
H2SO3+I2+H2O H2SO4+2HI 2FeCl3+2HI
H2SO4+2HI 2FeCl3+2HI 2FeCl2+2HCl+I2
2FeCl2+2HCl+I2
3FeCl2+4HNO3 2FeCl3+NO↑+2H2O+Fe(NO3)3
2FeCl3+NO↑+2H2O+Fe(NO3)3
| A.H2SO3>I->Fe2+>NO | B.I->Fe2+>H2SO3>NO |
| C.Fe2+>I->H2SO3>NO | D.NO>Fe2+>H2SO3>I- |
已知甲、乙、丙、X是4种中学化学中常见的物质,其转化关系如图所示。则甲和X不可能是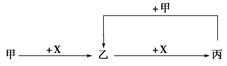
| A.甲为C,X为O2 |
| B.甲为SO2,X为NaOH溶液 |
| C.甲为Fe,X为Cl2 |
| D.甲为AlCl3溶液,X为NaOH溶液 |
下列是某同学对相应反应的离子方程式所作的评价,其中评价合理的是
| 编号 |
化学反应 |
离子方程式 |
评价 |
| A |
碳酸钙与醋酸反应 |
CO32-+2CH3COOH =2CH3COO-+H2O+CO2↑ |
错误,碳酸钙是弱电解质,不拆写 |
| B |
Ba(HCO3)2溶液中通入过量NaOH溶液 |
Ba2++HCO3-+OH-=BaCO3↓+H2O |
正确 |
| C |
碳酸氢钠的水解 |
HCO3-+H2O OH-+H2CO3 OH-+H2CO3 |
正确 |
| D |
等物质的量的FeBr2和Cl2反应 |
2Fe2++2Cl2=2Fe3++4Cl- |
正确 |
某溶液中有①NH4+、②Mg2+、③Fe2+、④Al3+四种离子,若向其中加入过量的氢氧化钠溶液,微热并搅拌,再加入过量盐酸,溶液中大量减少的阳离子是
| A.①② | B.①③ | C.②③ | D.③④ |
300 mL Al2(SO4)3溶液中,含Al3+为1.62 g,在该溶液中加入0.1 mol·L-1Ba(OH)2溶液300 mL(忽略溶液体积变化),反应后溶液中SO42-的物质的量浓度为
| A.0.4 mol·L-1 | B.0.1 mol·L-1 | C.0.2 mol·L-1 | D.0.3 mol·L-1 |
下列实验操作或装置符合实验要求的是