向四个体积相同的密闭容器中分别充入一定量的SO2和O2,开始反应时, 按正反应速率由大到小的顺序排列,正确的是
①500 ℃, 10 mol SO2和5 mol O2反应
②500 ℃, 用V2O5作催化剂, 10 mol SO2和5 mol O2反应
③450 ℃, 8 mol SO2和5 mol O2反应
④500 ℃, 8 mol SO2和5 mol O2反应。
| A.②①④③ | B.②①③④ | C.①②③④ | D.④③②① |
将物质的量均为0.1 mol K2SO4和Al2(SO4)3溶于水,向其中加入一定量的Ba(OH)2溶液,测得铝元素有一半留在溶液中,则生成BaSO4的物质的量可能为
| A.0.25 mol | B.0.30 mol | C.0.35 mol | D.0.4 mol |
VL Fe2(SO4)3溶液中含有ag SO42-,取此溶液0.5VL,用水稀释至2VL,则稀释后溶液中Fe3+的物质的量的浓度为
A.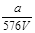 mol/L mol/L |
B.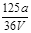 mol/L mol/L |
C.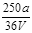 mol/L mol/L |
D.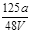 mol/L mol/L |
设NA表示阿伏加德罗常数的值。下列说法正确的是
| A.标准状况下,2.24 L CCl4中含Cl原子数目为0.4NA |
| B.白磷分子(P4)呈正四面体结构,12.4 g白磷中含有P-P键数目为0.6NA |
| C.1mol氯气参加氧化还原反应,转移的电子数一定为2 NA |
| D.5.6g Fe和足量的盐酸反应时,失去的电子数为0.3NA |
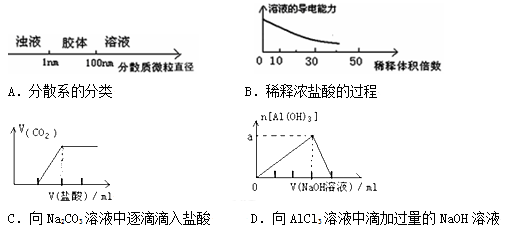
我们常用“往伤口上撒盐”来比喻某些人乘人之危的行为,其实从化学的角度来说,“往伤口上撒盐”的做法并无不妥,甚至可以说并不是害人而是救人。那么,这种做法的化学原理是
| A.胶体的电泳 | B.血液的氧化还原反应 |
| C.血液中发生复分解反应 | D.胶体的聚沉 |
将某些化学知识用图像表示,可以收到直观、简明的效果。下列图象所表示的化学知识中,明显不正确的是