配制1mol/L NaO H溶液100mL,填写下列空白
H溶液100mL,填写下列空白
(1)计算所需NaOH的质量 g
(2)用托盘天平称量NaOH
(3)将NaOH固体倒入 中溶解,并用玻璃棒不断搅拌
(4)待溶液冷却至室温,将其转移至100mL容量瓶中,此操作中 玻璃棒的作用是
玻璃棒的作用是
(5)用蒸馏水冲洗烧杯和玻璃棒2~3次,将洗涤液转移到容量瓶中。如果没有此操作,将导致所配制溶液浓度 (填偏高、偏低或无影响)
(6)向容量瓶中加水至刻度线下 1~2cm,改用 滴加,直至凹液面最低处与刻度线相切。在此操作中,如果俯视读数,将导致所配溶液的浓度 (填偏高、偏低或无影响)
1~2cm,改用 滴加,直至凹液面最低处与刻度线相切。在此操作中,如果俯视读数,将导致所配溶液的浓度 (填偏高、偏低或无影响)
(7)反复倒转容量瓶摇匀。如果摇匀后发现液面低于刻度线,又加水至刻度线,将导致所配溶液浓度 (填偏高、偏低或无影响)
查阅资料知:Br2的沸点为59℃,微溶于水,有毒性。某化学小组模拟工业流程从浓缩的海水中提取液溴,主要实验装置(夹持装置略去)及操作步骤如下:
①连接A与B,关闭活塞b、d,打开活塞a、c,向三颈瓶A中缓慢通Cl2至反应完全;
②关闭a、c,打开b、d,向A中鼓入足量热空气;
③进行步骤②的同时,向B中通入足量SO2;
④关闭b,打开a,再通过A向B中缓慢通入足量Cl2,完全反应;
⑤将B中所得液体进行蒸馏,收集液溴。
请回答:
(1)可以判断步骤①中反应已经完全的现象是 。
(2)步骤②中鼓入热空气的作用为 。
(3)步骤③中B容器里反应的化学方程式为 。
(4)本实验多次涉及尾气处理,可吸收处理B中尾气的是____________(填选项)。
| A.浓硫酸 | B.饱和NaCl溶液 | C.NaOH溶液 | D.水 |
(5)用C代替B,进行步骤①和②,此时C中有NaBr、NaBrO3等物质生成,该反应的化学方程式为 。
(6)继续向锥形瓶中滴加稀硫酸,经步骤⑤,也能制得液溴。与B装置相比,采用C装置的优点为 。
Ⅰ.某课外活动小组为了检验浓硫酸与木炭在加热条件下反应产生的SO2和CO2气体,设计了如图所示实验装置,a、b、c为止水夹,B是用于储气的气囊,D中放有用I2和淀粉的蓝色溶液浸湿的脱脂棉。
请回答下列问题
(1)对于易燃、易爆、有毒的化学物质,往往会在其包装上面贴上危险警告标签。浓硫酸的危险警告标签是 。
(2)装置A中发生反应的化学方程式为_______________________。
(3)此实验成败的关键在于控制反应产生气体的速率不能过快,因此设计了虚框部分的装置,则正确的操作顺序是_________________(用操作编号填写)
①向A装置中加入浓硫酸,加热,使A中产生的气体进入气囊B,当气囊中充入一定量气体时,停止加热;
②待装置A冷却,且气囊B的体积不再变化后,关闭止水夹a,打开止水夹b,慢慢挤压气囊,使气囊B中气体慢慢进入装置C中,待达到实验目的后,关闭止水夹b;
③打开止水夹a和c,关闭止水夹b;
(4)实验时,装置C中的现象为______________________________;
(5)当D中产生____________现象时,可以说明使E中澄清石灰水变浑浊的是CO2,而不是SO2;写出D中发生反应的化学方程式,并标出电子转移方向和数目______________。
Ⅱ. Cu与浓硫酸反应可得硫酸铜溶液。某学习小组将铜屑放入一定浓度的硫酸中,加热并不断鼓入空气也可得硫酸铜溶液,其反应原理为2Cu+O2+2H2SO4="=" 2CuSO4+2H2O。现欲将12.8g铜完全溶解,加蒸馏水后得200 mL溶液。计算:
(6)参加反应的氧气在标准状况下的体积是___________ L。(不必写计算过程)
(7)所得硫酸铜溶液的物质的量浓度是___________ mol/L(不必写计算过程)
某课外小组研究铝土矿中Al2O3的含量。查阅资料得知,铝土矿的主要成分是Al2O3,杂质是Fe2O3、SiO2等。从铝土矿中提取Al2O3的过程如下:
(1)固体B的主要用途有(写出1条即可) 。
(2)第①步,向铝土矿中加入足量烧碱溶液,充分反应,发生反应的离子方程式是: ; 。
(3)第③步中,生成氢氧化铝的离子方程式是 。 若往A溶液中通入足量CO2,请写出可能发生反应的离子方程式______________。
(4)工业上制取AlCl3用Al2O3与C、Cl2在高温条件下反应,每消耗0.5 mol碳单质,转移1 mol电子,反应的化学方程式是_____________________。
(5)将实验过程中所得固体精确称量。课外小组发现所得氢氧化铝固体的质量与原铝土矿质量相等,求该铝土矿中Al2O3的质量分数。(写出计算过程,计算结果保留一位小数)
在常温下,Fe与水并不起反应,但在高温下,Fe与水蒸气可发生反应。应用下列装置,在硬质玻璃管中放入还原铁粉和石棉绒的混合物,加热,并通入水蒸气,就可以完成高温下“Fe与水蒸气的反应实验”,并收集纯净干燥的气体。请回答该实验中的问题。
(1)写出该反应的化学方程式 ;干燥剂是_________(写名称)。
(2)圆底烧瓶中盛装的水,该装置受热后的主要作用是 ;烧瓶底部放置了几片碎瓷片,其作用是 。
(3)试管中收集气体是 (写化学式),如果要在A处玻璃管处点燃该气体,则必须对该气体进行 。在虚线框内画出收集该气体的装置图。(限选仪器:试管、玻璃导管、水槽)
(4)反应后得到黑色固体,主要成分是Fe3O4,还含有少量Fe和FeO;限选以下试剂:稀HNO3、稀HCl、KSCN溶液、氯水、CuSO4溶液;
设计实验方案检验所得固体中含有Fe3O4,写出实验步骤和实验现象_____________。
‚证明固体中含有没完全反应的Fe____________________________。
根据题目要求填空:
(1)硫、氮的氧化物是主要的大气污染物,对大气的影响之一是导致酸雨。用化学方程式表示NO2形成酸雨的原因: ,该反应中氧化剂和还原剂的物质的量之比为 。
(2)实验室常用的几种气体发生装置如图A、B、C所示: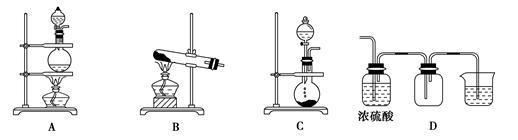
实验室可以用B或C装置制取氨气,如果用B装置,反应的化学方程式是______________;如果用C装置,通常使用的药品是______________(写名称);
‚下图是某学生设计收集氨气的几种装置,其中可行的是______________。
ƒ若用A装置与D装置相连制取并收集X气体,则X可能 是下列气体中的_____________
A.CO2B.NOC.Cl2D.H2
写出A装置中反应的离子方程式_______________。
(3)氢化钠(NaH)是一种还原性极强的物质,广泛应用于工业生产。
氢化钠(NaH)中Na元素的化合价为+1,在高温下氢化钠(NaH)可将四氯化钛(TiCl4)还原成金属钛,该反应的化学方程式为 。
‚NaH能与水剧烈反应:NaH+H2O===NaOH+H2↑,NaH与液氨(NH3)也有类似反应,该反应的化学方程式为_________________________。
如果有12g NaH参加此反应,则转移电子的物质的量为________mol
(4)用SiHCl3与过量H2反应制备纯硅的装置如图所示(热源及夹持装置均已略去):
SiHCl3遇水剧烈反应生成H2SiO3、HCl和另一种物质,写出配平的化学反应方程式:_____________;H2还原SiHCl3过程中若混入O2,可能引起的后果是___________;